
科目: 来源: 题型:
关于化学键的下列说法正确的是 ( )
A.构成离子晶体的作用力可能是离子键也可能是共价键
B.氯化铯晶体是由氯化铯分子构成的
C.由于离子的带电量有限,一个离子可以同时吸引的带相反电荷的离子数也有限
D.一种离子化合物如果适合作耐高温材料,它的晶格能一定相当大
查看答案和解析>>
科目: 来源: 题型:
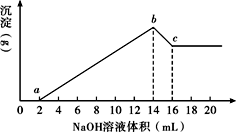 将一定质量的Mg、Al合金全部溶解在500 mL盐酸中(体积变化不计),取10 mL反应后的溶液,用1 mol/L NaOH溶液滴定得下图关系。
将一定质量的Mg、Al合金全部溶解在500 mL盐酸中(体积变化不计),取10 mL反应后的溶液,用1 mol/L NaOH溶液滴定得下图关系。
(1)求Mg、Al质量各是多少?
(2)求盐酸的物质的量浓度为多少?
查看答案和解析>>
科目: 来源: 题型:
能正确表示下列反应的离子方程式是
A.足量硫化氢气体通入硫酸铁溶液中:H2S+Fe3+=Fe2++S↓+2H+
B.足量铁与稀硝酸反应:Fe+4H++NO3-=Fe2++4H2O+NO↑
C.醋酸溶液与纯碱反应:CO32- +2H+=+H2O+CO2↑
D.等物质的量的Ba(OH)2与NaHSO4在溶液中反应:
Ba2++OH-+H++SO42-=BaSO4↓+H2O
查看答案和解析>>
科目: 来源: 题型:
下图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料。
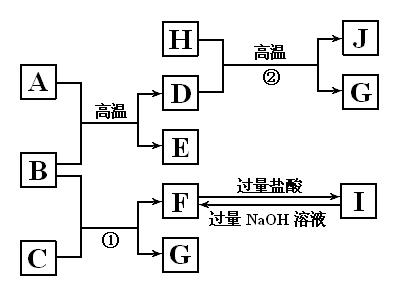
根据图示回答问题:
(1)写出下列物质的化学式:A ,E ,I ;
(2)反应①的化学方程式是 ;
反应②的化学方程式是 ;
(3)J与盐酸反应的化学方程式是 ;
反应后的溶液与D反应的化学方程式是 。
查看答案和解析>>
科目: 来源: 题型:
下列有关叙述正确的是
①碱金属单质的密度通常情况下均比水小 ![]()
②碱金属元素均具有强还原性 ![]()
③碱金属的氢氧化物在加热的条件下均不分解 ![]()
④热稳定性:Na2CO3>NaHCO3>H2CO3 ![]()
⑤CsOH是离子化合物,易溶于水,且碱性比NaOH强 ![]()
⑥Cs2CO3加热易分解成Cs2O和CO2 ![]()
⑦Na、K、Rb、Cs中,Cs的熔点最高,密度最大 ![]()
A.全部 B.全不正确 C.④⑤ D.①②④⑤⑦![]()
查看答案和解析>>
科目: 来源: 题型:
下列实验能成功的是( )
A、苯与浓溴水反应(Fe作催化剂)制溴苯
B、福尔马林与苯酚的混合物,沸水浴加热制酚醛树脂
C、氯乙烯加聚的生成物能使酸性KMnO4溶液褪色
D、加热硫酸、乙醇、氯化钠固体的混合物制氯乙烷
查看答案和解析>>
科目: 来源: 题型:阅读理解
A.已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为 。
(2)B的氢化物的分子空间构型是 。其中心原子采取 杂化。
(3)写出化合物AC2的电子式 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为 。
(4)E的核外电子排布式是 ,ECl3形成的配合物的化学式为 。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是 。
B.醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷和1-溴丁烷的反应如下:
NaBr+H2SO4![]() HBr+NaHSO4 ①
HBr+NaHSO4 ①
R-OH+HBr![]() R-Br+H2O ②
R-Br+H2O ②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br—被浓硫酸氧化为Br2等。有关数据列表如下;
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g·cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
请回答下列问题:
(1)溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是 。(填字母)
a.圆底烧瓶 b.量筒 c.锥形瓶 d.布氏漏斗
(2)溴代烃的水溶性 (填“大于”、“等于”或“小于”);其原因是
。
(3)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在 (填“上层”、“下层”或“不分层”)。
(4)制备操作中,加入的浓硫酸必需进行稀释,起目的是 。(填字母)
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(5)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是 。(填字母)
a.NaI b.NaOH c.NaHSO3 d.KCl
(6)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于 ;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是 。
查看答案和解析>>
科目: 来源: 题型:
有V L乙炔和乙烯的混合气体,在催化剂的作用下与足量H2发生加成反应,共消耗H2 1.25V L,则原混合气中乙炔和乙烯的体积比为( )
A.3∶1 B.2∶1 C.1∶1 D.1∶3
查看答案和解析>>
科目: 来源: 题型:
CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属离子型碳化物,请通过对CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应产物正确的是( )
A.ZnC2水解生成乙烷(C2H6) B.Al4C3水解生成丙炔(C3H4)
C.Mg2C3水解生成丙炔(C3H4) D.Li2C2水解生成乙烯(C2H4)
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏加德罗常数,下列说法正确的是( )
![]() A.23gNa在氧气中完全燃烧失电子数为0.5NA
A.23gNa在氧气中完全燃烧失电子数为0.5NA
![]() B.1L2mol·L-1的MgCl2溶液中含Mg2+数为2NA
B.1L2mol·L-1的MgCl2溶液中含Mg2+数为2NA
![]() C.标准状况下,11.2LSO3所含分子数为0.5NA
C.标准状况下,11.2LSO3所含分子数为0.5NA
![]() D.室温下,8g甲烷含有共价键数为2NA
D.室温下,8g甲烷含有共价键数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com