
科目: 来源: 题型:
已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液形成无色溶液,其化学方程式是PbSO4+2CH3COONH4====Pb(CH3COO)2+(NH4)2SO4。当在醋酸铅溶液中通入H2S时,有黑色沉淀PbS生成,表示这个反应的有关离子方程式正确的是( )
A.Pb(CH3COO)2+H2S====PbS↓+2CH3COOH
B.Pb2++H2S====PbS↓+2H+
C.Pb2++2CH3COO-+H2S====PbS↓+2CH3COOH
D.Pb2++2CH3COO-+2H++S2-====PbS↓+2CH3COOH
查看答案和解析>>
科目: 来源: 题型:
现有电解质溶液:①Na2CO3 ②NaHCO3
③NaAlO2 ④CH3COONa ⑤NaOH。
(1)当五种溶液的pH相同时,其物质的量浓度由大到小的顺序是__________(填编号)。
(2)将上述物质的量浓度均为0.1 mol·L-1的五种溶液,稀释相同倍数时,pH变化最大的是__________(填编号)。
(3)在上述五种电解质溶液中,分别加入AlCl3溶液,无气体产生的是__________(填编号)。
(4)将上述①②③④四种电解质溶液混合,发生反应的离子方程式为__________。
查看答案和解析>>
科目: 来源: 题型:
为了提高煤燃烧的热效率并减少SO2和烟尘对大气的污染,适宜采取的措施是( )
A.通入大量的空气 B.将煤块粉碎成煤粉
C.将煤制成多孔的煤球 D.将煤经过处理,转化为气体燃料
查看答案和解析>>
科目: 来源: 题型:
下列关于反应能量的说法正确的是( )
A.Zn(s)+CuSO4(aq)====ZnSO4(aq)+Cu(s) ΔH=-216 kJ·mol-1,E反应物<E生成物
B.CaCO3(s)====CaO(s)+CO2(g)
ΔH=+178.5 kJ·mol-1,
E生成物>E反应物
C.HI(g)====![]() +
+![]()
ΔH=-26.5 kJ·mol-1,1 mol HI在密闭容器中分解达平衡时放出26.5 kJ的能量
D.H+(aq)+OH-====(aq)H2O(l) ΔH=-57.3 kJ·mol-1,1 L 1 mol·L-1的NaOH溶液与含0.5 mol H2SO4的浓硫酸混合后放热57.3 kJ
查看答案和解析>>
科目: 来源: 题型:阅读理解
某学校化学兴趣小组同学在两支小试管中分别加入浓度为4 mol·L-1稀盐酸3 mL,将分别装有0.3 g NaHCO3和0.3 g Na2CO3粉末的小气球分别套在两支试管口。将气球内的NaHCO3和Na2CO3同时倒入试管中,观察到的现象及分析如下:
(1)比较两支试管中的现象:_______________________________。
(2)若两气球内的压强相同,两试管大小相同,则大小气球体积之比约为_____________(填最简整数比)。
(3)甲同学用手触摸试管,发现盛NaHCO3粉末的试管变冷,而盛Na2CO3的试管温度升高。由此他得出:不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应。甲同学写出了下列热化学方程式(其中“aq”代表水合或无限稀释的含义):
![]() (aq)+H+(aq)====H2O(l)+CO2(g);ΔH>0;
(aq)+H+(aq)====H2O(l)+CO2(g);ΔH>0;
![]() (aq)+2H+(aq)====H2O(l)+CO2(g);ΔH<0;甲分析结论的方法是否科学?__________。(填“是”或“否)
(aq)+2H+(aq)====H2O(l)+CO2(g);ΔH<0;甲分析结论的方法是否科学?__________。(填“是”或“否)
(4)为研究反应是吸热还是放热,乙同学继续进行下列实验。(每个实验平行做三次,取平均值)
| 序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后最高或最低温度 |
| 1 | 35 mL 水 | 2.5 g NaHCO3固体 | 20 ℃ | 18.5 ℃ |
| 2 | 35 mL水 | 3.2 g Na2CO3固体 | 20 ℃ | 24.3 ℃ |
| 3 | 35 mL稀盐酸含 | 2.5 g NaHCO3的饱和溶液32.5 mL | 20 ℃ | 19 ℃ |
| 4 | 35 mL稀盐酸含 | 3.2 g Na2CO3的饱和溶液23.1 mL+10 mL水 | 20 ℃ | 24.2 ℃ |
| 5 | 35 mL稀盐酸 | 2.5 g NaHCO3固体 | 20 ℃ | 16.2 ℃ |
| 6 | 35 mL稀盐酸 | 3.2 g Na2CO3固体 | 20 ℃ | 25.1 ℃ |
请你帮助填写相关内容:
①该研究报告的题目是《_______________________》。
②通过上述实验可得出五条结论:
a.NaHCO3的溶解是__________(“吸热”或“放热”)过程;
b.Na2CO3的溶解是____________(“吸热”或“放热”)过程;
c.NaHCO3的饱和溶液和盐酸的反应是___________(“吸热”或“放热”)反应;
d.Na2CO3的饱和溶液和盐酸的反应是____________(“吸热”或“放热”)反应;
e.NaHCO3固体与稀盐酸反应的反应热是__________(填a→d的字母)的热效应之和。
查看答案和解析>>
科目: 来源: 题型:
石油、天然气、煤等在地球上的蕴藏量是有限的,因此:①可以利用电解水的方法得到氢气作能源 ②可用酒精作能源 ③砍伐树木作能源 ④应开发太阳能、核能等新能源。上述说法正确的是( )
A.只有① B.①和④ C.②和③ D.④
查看答案和解析>>
科目: 来源: 题型:
铊(Tl)是某超导材料的组成元素之一,与铝同族,位于第6周期。Tl3+与Ag在酸性介质中发生反应:Tl3++2AgTl++2Ag+。下列推断正确的是( )
A.Tl+的最外层有1个电子
B.Tl3+的氧化性比Al3+弱
C.Tl能形成+3价和+1价的化合物
D.Tl+的还原性比Ag强
查看答案和解析>>
科目: 来源: 题型:
最近我国某近代物理研究所取得重大科研成果,研制出首批氧18气体(18O2),氧18是一种稳定的氧的同位素,称为重氧。下列有关说法正确的是( )
A.1.8 g氧18气体的物质的量是0.1 mol
B.0.1 mol重氧水H218O所含的中子数为6.02×1023
C.0.2 mol氧18气体的体积约为4.48 L
D.氧18气体的摩尔质量是36 g
查看答案和解析>>
科目: 来源: 题型:
W、X、Y、Z为短周期中除稀有气体以外的四种元素,它们的原子序数依次增大。其中只有Y为金属元素,Y和W的最外层电子数相等,W和Z可组成化学式为W2Z的化合物,Y、Z两元素原子的质子数之和为W、X两元素原子的质子数之和的3倍。由此推断:
(1)W、X、Y、Z的元素符号分别为__________、__________、__________、__________。
(2)W2Z是由__________键形成的分子,其电子式为__________________。
(3)由Y、X、W形成的物质中有__________键和__________键形成的__________化合物。
查看答案和解析>>
科目: 来源: 题型:
木炭与浓硫酸在加热条件下发生反应:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O↑,下图虚线框中的装置可用来检验该反应产生的所有气体产物,请完成下列问题:
CO2↑+2SO2↑+2H2O↑,下图虚线框中的装置可用来检验该反应产生的所有气体产物,请完成下列问题:
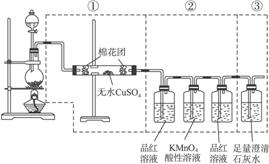
(1)如果装置中①②③三部分仪器的连接顺序改变②①③,则可以检出的物质是___________;不能检出的物质是___________。
(2)如果将仪器的连接顺序变为①③②,则可以检出的物质是___________;不能检出的物质是___________。
(3)如果将仪器的连接顺序变为②③①,则可以检出的物质是___________;不能检出的物质是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com