
科目: 来源: 题型:
“神州”六号飞船上使用是氢氧燃料电池,其电池总反应式为![]()
试完成下列问题:
若电解溶液为![]() 溶液,则电极反应式为:
溶液,则电极反应式为:
负极:
正极:
(2)如果把![]() 改为稀硫酸做导电物质,则电极反应式为:
改为稀硫酸做导电物质,则电极反应式为:
负极:
正极:
(3)如果把![]() 改为
改为![]() ,
,![]() 溶液作导电物质,则电极反应式为:
溶液作导电物质,则电极反应式为:
负极:
正极:
查看答案和解析>>
科目: 来源: 题型:
. 氨是一种重要的化工原料,某学习小组欲制取氨气并探究其性质。请回答:
(1)实验室制取氨气的化学方程式是 。
(2)①右图是进行氨气喷泉实验的装置,引发喷泉的操作步骤是 。

②氨气使烧杯中溶液由无色变为红色,其原因是_______________________________(用电离方程式表示)。
(3)该小组同学设计了下图所示的实验装置(部分夹持仪器未画出),探究氨气的还原性并检验产物。

① 实验现象为:黑色CuO变为红色;白色无水CuSO4粉末变为蓝色;同时生成一种无色气体,该气体无污染。请写出氨气与CuO反应的化学方程式 。
② 碱石灰的作用是 。
③该装置存在明显缺陷,请指出存在的问题并提出改进意见
。
(4)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:Cu2O是一种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(Cu+![]() Cu + Cu2+)。
Cu + Cu2+)。
请你设计一个简单的实验检验该红色物质中是否含有Cu2O。
;
(5)工业废气中的氮氧化物是主要的大气污染物之一。为了治理污染,工业上常用氨气与之发生反应:NOx+NH3→N2+H2O,使其转化为无毒的N2 。现有NO2和NO的混合气体3.0 L,跟3.4 L(同温同压下)NH3反应,恰好使其全部转化为氮气,则原混合气体中,NO2与NO的体积比是__________。
查看答案和解析>>
科目: 来源: 题型:
北京奥运会主体育场“鸟巢”运用了高强度、高性能的钒氮合金钢和透明的ETFE膜,并采用新一代的LED高亮度氮化镓材料。下列有关说法不正确的是
A.合金的熔点通常比组分金属低,硬度比组分金属高
B.用金属铝与V2O5反应冶炼钒,主要是因为铝的还原能力比钒弱
C.已知Ga处于IIIA族,可推知氮化镓化学式为GaN
D.ETFE膜( [CH2-CH2-CF2-CF2 ]n)是由两种单体加聚而成的
查看答案和解析>>
科目: 来源: 题型:
一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)![]() CH3OH(g) 。反应过程中生成甲醇的物质的量与温度、时间的变化曲线如图所示
CH3OH(g) 。反应过程中生成甲醇的物质的量与温度、时间的变化曲线如图所示
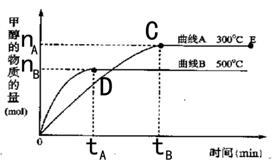
根据题意完成下列各题:
(1)在300℃,从反应开始到平衡,氢气的平均反应速率v(H2)= (用 nA 和tA 表示)。
(2)根据图示曲线判断合成甲醇的反应为 (填“吸热”或“放热”)反应,理由是 。
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是 ( )
A.正、逆反应速率均加快 B.CO的浓度减少
C.甲醇的物质的量减少 D.重新平衡时n(CH3OH) / n(H2)增大
(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:
(用化学方程式表示)
查看答案和解析>>
科目: 来源: 题型:
[化学——选修化学与技术]
技术的发展与创新永无止境。我国化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下图所示:
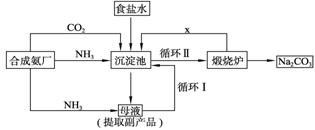
(1)向沉淀池中要通入CO2和氨气,应先通入__________(填化学式),原因是__________。
(2)沉淀池中发生反应的化学方程式是__________。
(3)母液中的溶质主要是__________,向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用是__________。
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了__________(填上述流程中的编号)的循环;物质x是__________,从沉淀池中提取沉淀的操作是__________。
(5)写出煅烧炉中发生反应的化学方程式__________。
(6)这样制得的产品碳酸钠中可能含有的杂质是__________(填化学式),为检验该杂质的存在,具体操作是__________。
查看答案和解析>>
科目: 来源: 题型:
下列关于N、Si、S、Cl等非金属元素化合物的说法正确的是 ( )
A.硝酸与金属反应时,硝酸越稀其还原产物中氮元素的价态越低
B.二氧化硅是制造太阳能电池板的主要材料
C.少量SO2与Na2O2反应的方程式为:2SO2+2Na2O2=2Na2SO3+O2
D.Ca(ClO)2比HClO稳定,所以漂白粉露置在空气中不会失效
查看答案和解析>>
科目: 来源: 题型:
若过程I与过程II温度相同,则关于反应 N2O4(g) ![]() 2NO2 (g)在下列过程中发生的变化描述正确的是
2NO2 (g)在下列过程中发生的变化描述正确的是

A.a'<b',a>b B.在平衡I向平衡II过渡的过程中,v(逆)>v(正)
C.a'=a, b'=b D.平衡II与平衡IV中N2O4的质量分数相等
查看答案和解析>>
科目: 来源: 题型:
BAD是一种紫外线吸收剂,其合成方法如下:

已知:
Ⅰ、B分子中所有H原子的化学环境相同;
Ⅱ、BAD的结构为: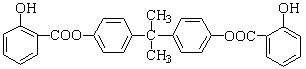 。
。
请回答下列问题:
⑴ A的名称为 。
⑵ F的结构简式为 。F的一些同分异构体能使氯化铁溶液变色,能发生银镜反应,且苯环上的一硝基取代产物有两种。符合上述条件的同分异构体有 种。
⑶ 反应②的化学方程式为 ;反应③在一定条件下能直接进行,其反应类型为 。
⑷ G是一种氨基酸,且羧基和氨基处于苯环的对位。写出G缩聚产物可能的结构简式 (只要求写一种)。
查看答案和解析>>
科目: 来源: 题型:
某研究性学习小组从网上查到绿矾(FeSO4·7H2O)受热分解的方程式为:
2FeSO4·7H2O![]() Fe2O3+SO3↑SO3↑+14H2O↑,就设计了如下实验装置来验证绿矾受热分解是否发生上述反应。
Fe2O3+SO3↑SO3↑+14H2O↑,就设计了如下实验装置来验证绿矾受热分解是否发生上述反应。
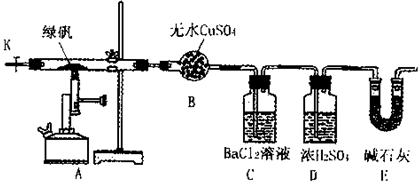
主要实验步骤如下:
①组装仪器并检查装置的气密性;
②称量绿矾样口及U型干燥管E的质量,将称量后的绿矾置于硬质玻璃管内;
③关闭活塞K,加强热使绿矾完全分解;
④打开活塞K,缓缓鼓入一定量的氮气;
⑤再次称量干燥管E的质量;
⑥重复④⑤的操作,直到干燥管E的质量基本不变为止;
⑦称量洗气瓶C中所得沉淀的质量。
试回答:
(1)洗气瓶D中浓H2SO4的作用为: ;
(2)步骤⑦从溶液中获取生成沉淀质量的具体操作为: ;
(3)实验小组的报告如下,请补充完整:
| 实验记录 | 分析或计算结果 | |
| 现象 | 硬质管内绿色变为红棕色; | 生成物有 |
| 干燥管B中晶体白色变蓝色。 | 生成物有H2O | |
| 数据 | 称取绿矾样品16.68g; | 反应的绿矾0.06mol |
| 干燥管E最后增重2.24g; | 生成SO2 mol | |
| C中生成白色沉淀的质量为4.66g; | 生成DO3 0.02mol |
(4)该实验所得到的数据与所样到的化学方程式中的定量关系不相符合,请分析可能的原因。
(5)为达到“验证绿矾受热分解是否发生上述反应”的目的,该实验的设计有多处不妥,请提出改进建议(两条即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com