
科目: 来源: 题型:
Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法中正确的是 ( )
A.Na2O2只作氧化剂
B.Na2FeO4既是氧化产物又是还原产物[
C.O2是还原产物
D.2 mol FeSO4发生反应时,反应中共有8 mol电子转移
查看答案和解析>>
科目: 来源: 题型:
![]() 向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。
![]() 向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的
向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的![]() 沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是
沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是
![]() A.
A.![]() B.
B.![]() C.n=m+17Vc D.
C.n=m+17Vc D. ![]() m<
m<![]() <
<![]()
查看答案和解析>>
科目: 来源: 题型:
金属材料在日常生活以及生产中有着广泛的运用。下列关于金属的一些说法不正确的是
A.合金的性质与其成分金属的性质不完全相同
B.工业上金属Mg、Al都是用电解熔融的氯化物制得的
C.金属冶炼的本质是金属阳离子得到电子变成金属原子
D.越活泼的金属越难冶炼
查看答案和解析>>
科目: 来源: 题型:
|
A.金属氧化物一定是碱性氧化物,非金属氧化物一定是酸性氧化物
B.难溶于水的电解质一定是弱电解质
C.离子化合物中可能含有共价键
D.由同种元素组成的物质一定属于纯净物
查看答案和解析>>
科目: 来源: 题型:
前不久报道,我国“煤变油”技术已进入世界先进行列,科学家通过不懈努力,找到了![]() (由煤和水蒸气高温制得)应用的新方法,如:
(由煤和水蒸气高温制得)应用的新方法,如:
(1)合成汽油:![]() 和
和![]() 在443—473K的温度下用钴作催化剂,可合成碳原子数为5—8的烷烃。
在443—473K的温度下用钴作催化剂,可合成碳原子数为5—8的烷烃。
①写出 CO合成汽油![]() 的化学方程式
的化学方程式
②若向密闭的合成塔里通入恰好能完全反应的CO和![]() ,当完全反应时,气压降至原来的2/5,(温度不变),此时 (填“有”或“没有”)汽油生成,理由是
,当完全反应时,气压降至原来的2/5,(温度不变),此时 (填“有”或“没有”)汽油生成,理由是
③要达到上述合成汽油的要求,CO和![]() 的体积比的取值范围是
的体积比的取值范围是
(2)合成甲醇:在390°C、3.03×105Pa时,![]() ,以n表示
,以n表示![]() 和
和![]() 的物质的量之比,a表示
的物质的量之比,a表示![]() 的转化率,x表示达到反应限度时混合物中
的转化率,x表示达到反应限度时混合物中![]() 的体积分数,则
的体积分数,则![]() 、a、x的关系式为 。
、a、x的关系式为 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
近年来,碳和碳的化合物在生产生活实际中应用广泛。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知:① 2 CH4 (g) + 3O2 (g) = 2 CO (g) + 4 H2O(l) △H1 = -1214.6 KJ/mol
② 2 CO (g) + O2(g) = 2 CO2 (g) ΔH2 = -566 kJ/mol
则反应CH4(g) + 2 O2 (g) = CO2 (g) + 2 H2O (l) 的△H = 。
(2)将两个石墨电极插人KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。通入CH4的一极,其电极反应式是:CH4 + 10 OH―― 8e-= CO32-+ 7 H2O;通入O2的一极,其电极反应式是 。
(3)若用石墨做电极电解500 ml饱和食盐水,写出电解反应的离子方程式为: ;电解一段时间后两极共收集到标准状况下的气体1.12 L(不考虑气体的溶解)。停止通电,假设反应前后溶液体积不变,则所得溶液的pH= 。
(4)将不同量的CO (g) 和H2O (g) 分别通入到体积为2 L的恒容密闭容器中,进行反应
CO (g) + H2O (g) ![]() CO2 (g) + H2 (g),得到如下三组数据:
CO2 (g) + H2 (g),得到如下三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| H2O | CO | CO2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
① 实验1中以υ(H2) 表示的反应速率为 。
② 实验2中的平衡常数是 (计算结果保留两位小数)。
③ 该反应的正反应为 (填“吸”或“放”)热反应。
④ 若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),
则a、b应满足的关系是 (用含a、b的数学式表示)。
查看答案和解析>>
科目: 来源: 题型:
已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g) ΔH=-226 kJ/mol
根据以上热化学方程式判断,下列说法正确的是
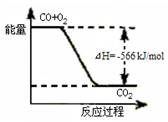
A.CO的燃烧热为283 kJ
B.右图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
查看答案和解析>>
科目: 来源: 题型:
在下图转化关系中,固体甲的焰色反应呈黄色,M为常见的液体物质,酸G是重要的化工产品和化工原料;固体H能溶解在A溶液和酸G中,且H为良好的耐火材料(图中部分产物没有列出)。

(1)写出M和过量的固体甲反应的化学方程式:
(2)如图表示的是生产酸G的工业流程:

①设备乙的名称为 ;
②气体X的主要成分为 ;
③写出设备甲中常见的化学反应 ;
(3)固体乙与M反应的化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
[化学——选修物质结构与性质]
A、B、C、D为1~36号元素。A元素的原子价电子排带为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的p亚层中有3个未成对电子,D元素原子核外的M层中只有2对成对电子。
(1)当n=2时,AB2属于_____分子(填“极性”或“非极性”),分子中有____个σ键,____个π键。
(2)当n=3时,A与B形成的晶体属于_____晶体。
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种元素的第一电离能由大到小的顺序是___(用元素符号表示)。
(4)已知某红紫色配合物的组成为CoCl3·5NH3·H2O。该配合物中的中心离子钴离子在基态的核外电子排布式为____,作为配位体之一的NH3分子的空间构型为_____。
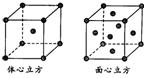
(5)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为_____。
查看答案和解析>>
科目: 来源: 题型:
下列反应的离子方程式正确的是 ( )
A.苯酚钠溶液中通入少量CO2:CO2 + H2O + C6H5O-→C6H5OH + HCO3-
B.浓盐酸与MnO2反应制取氯气:MnO2+2H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
C.向NaAlO2溶液中通入少量CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-![]()
D.用惰性电极电解氯化镁溶液:2Cl-+ 2H2O ![]() H2↑+ Cl2↑+2OH-
H2↑+ Cl2↑+2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com