
科目: 来源: 题型:
下列对“摩尔(mol)”的叙述不正确的是
A.摩尔是一个单位,用于计量物质所含微观粒子的多少
B.摩尔既能用来计量纯净物,又能用来计量混合物
C.1 mol任何气体所含的气体分子数目都相等
D.用“摩尔”(而不用“个”)计量微观粒子与用“纳米”(而不用“米”)计量原子直径,计量思路都是扩大单位
查看答案和解析>>
科目: 来源: 题型:
实验室制取SO2的反应原理为:Na2SO3+H2SO4(较浓)====Na2SO4+SO2↑+H2O。请用下列装置设计一个实验,以测定SO2转化为SO3的转化率。
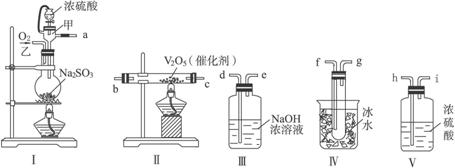
(1)这些装置的连接顺序(按气体左右的方向)是_________→_________→_________→
_________→_________→_________→_________→(填各接口的编号)。
(2)实验时甲仪器的作用与原理是
_________________________________________________。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是____________。
(4)Ⅳ处观察到的现象是_____________________________________________。
(5)用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重m g,则本实验中SO2的转化率为___________。
查看答案和解析>>
科目: 来源: 题型:
20 ℃时,将a g硝酸钾溶于b g水中,恰好形成V mL饱和溶液。下列关于该溶液的关系式错误的是
A.c(KNO3)=![]() mol·L-1
mol·L-1
B.质量分数:w(KNO3)=![]() %
%
C.20 ℃时硝酸钾的溶解度:S=![]() g
g
D.密度:ρ=![]() g·L-1
g·L-1
查看答案和解析>>
科目: 来源: 题型:
(2008·上海)生态农业涉及农家废料的综合利用,某种肥料经发酵得到一种含甲烷、二氧化碳、氮气的混合气体。2.016L(标准状况)该气体通过盛有红热CuO粉末的硬质玻璃管,发生的反应为:CH4+4CuO![]() CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通入足量的澄清石灰水中,充分反应吸收,生成沉淀8.5g,则:
CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通入足量的澄清石灰水中,充分反应吸收,生成沉淀8.5g,则:
(1)原混合气体中甲烷的物质的量是 。
(2)原混合气体中氮气的体积分数为多少?(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
下列反应有电子转移,同时溶液的颜色又发生变化的是
A.FeCl3溶液中加入一定量的Zn粉
B.铁片放入CuSO4溶液中
C.FeCl3溶液加入NaOH溶液中
D.NaOH溶液中加入铝片
查看答案和解析>>
科目: 来源: 题型:
某铝合金中含有合金元素镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验,请完成有关问题:
(1)称取样品a g,称量时应该使用的主要仪器的名称是
_______________________________。
(2)将样品溶解于足量的稀盐酸,过滤。滤液中主要含有______________________________,滤渣中含有_______________________,溶解、过滤用到的玻璃仪器是__________________。
(3)滤液中加过量氢氧化钠溶液、过滤。有关的离子方程式是_______________________,____________________________________。
(4)步骤(3)的滤液中通入足量二氧化碳气体,过滤。有关的离子方程式是______________。
(5)步骤(4)过滤后的滤渣用蒸馏水洗涤数次,烘干并灼烧至恒重,冷却后称重,其质量为b g。有关的化学方程式是____________________,原样品中铝的质量分数是_________。
(6)若步骤(3)中加入氢氧化钠的量不足,则实验结果偏___________(“高”“低”或“不影响”,下同);若步骤(5)中滤渣没有洗涤,则实验结果偏___________;若滤渣灼烧不充分,则实验结果偏___________。
查看答案和解析>>
科目: 来源: 题型:
除去SiO2中混有的少量生石灰和石灰石,有如下操作:①加水溶解 ②加水煮沸 ③过滤 ④加稀HCl ⑤加稀H2SO4,正确的操作顺序是
A.①③ B.④③ C.⑤③ D.②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com