
科目: 来源: 题型:
塑料制品废弃物严重污染环境,常称为“白色污染”。为了防止这种污染,一条重要途径是将合成高分子化合物重新变成小分子化合物。目前,对结构为
![]() 的物质已成功实现了这种处理。试分析,若用CH3OH来处理它,得到的有机物可能是 …( )
的物质已成功实现了这种处理。试分析,若用CH3OH来处理它,得到的有机物可能是 …( )
A.![]() B.HO—CH2CH2—COOH
B.HO—CH2CH2—COOH

查看答案和解析>>
科目: 来源: 题型:
已知α氨基酸能与亚硝酸反应得到α羟基酸。例如:
![]()
![]()
现有某α氨基酸盐A,其分子中原子数之比为C∶H∶O∶N=3∶10∶2∶2,由它开始有如下图所示的反应关系,其中无机产物均已略去,括号中的数字为其相对分子质量。
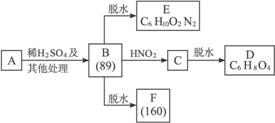
(1)写出下列有机物结构简式:D__________,E__________,F__________。
(2)写出下列转化的化学方程式:
①B→C______________________________,
②A→B______________________________。
查看答案和解析>>
科目: 来源: 题型:
乙醛在催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末,试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60—80 ℃时,用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次,反应基本完全。有关物质的沸点如下:
| 物质 | 乙醛 | 乙酸 | 甘油 | 水 |
| 沸点/℃ | 20.8 | 117.9 | 290 | 100 |
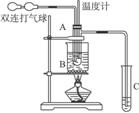
请完成下列问题:
(1)试管A内在60—80 ℃时发生的主要反应的化学方程式为(注明反应条件)________
____________。
(2)如图所示,在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在___________;当试管A内主要反应完成后,温度计水银球的位置应在___________,目的是_______________________________。
(3)烧杯B的作用是____________________________________;烧杯B内盛装的液体可以是____________________(选填“甘油”或“水”)。
(4)若想检验试管C中是否含有产物乙酸,请你在所提供的药品中进行选择,设计一个简便的实验方案。
所提供的药品有:pH试纸,红色的石蕊试纸,白色的醋酸铅试纸,碳酸氢钠粉末。实验仪器任选。
该方案为(简述操作过程):____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z三种元素核电荷数在11-17之间,它们的最高价氧化物对应的水化物是HXO4、H2YO4、H3ZO4, 则下列判断正确的是( )
A. 原子半径X>Y>Z
B. 酸性: H3ZO4>H2YO4>HXO4
C. 稳定性: HX>H2Y>ZH3
D. 非金属性: X<Y<Z
查看答案和解析>>
科目: 来源: 题型:
酚酞是常用的酸碱指示剂,结构简式为:
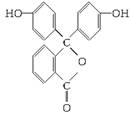
(1)酚酞的分子式为______________________________。
(2)酚酞属于_____________________、________________类衍生物。
(3)酚酞分别在1 mol·L-1 HCl和1 mol·L-1 NaOH溶液中溶解,在_____________中的溶解度大,原因是_________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(1)下图是一套实验室制取气体的装置,用于发生、干燥和收集气体。下列各组物质中能用这套装置进行实验的是_____________(填编号)。

A.MnO2和浓盐酸 B.Zn和稀硫酸
C.MnO2和H2O2 D.CaCO3和盐酸
(2)将过氧化氢溶液滴入含有酚酞的氢氧化钠溶液中,红色消失。甲同学认为这是因为过氧化氢是二元弱酸(H2O2![]() H++
H++![]() )消耗了OH-,而使酚酞褪色;乙同学认为,过氧化氢具有强氧化性,将酚酞氧化,红色消失。试设计一个简单易行的实验验证甲、乙两同学的解释哪个正确。
)消耗了OH-,而使酚酞褪色;乙同学认为,过氧化氢具有强氧化性,将酚酞氧化,红色消失。试设计一个简单易行的实验验证甲、乙两同学的解释哪个正确。
(3)久置的油画的白色部位(化学成分为PbSO4)常会变黑(化学成分为PbS),用双氧水擦拭后又可恢复原貌,则发生反应的化学方程式为____________________________。
查看答案和解析>>
科目: 来源: 题型:
微量元素硒对人体有很大作用。已知硒与氧同主族,与钾同周期。下列有关硒元素性质的叙述错误的是( )
A.单质硒既能溶于盐酸又能溶于烧碱溶液,且均产生氢气
B.硒的最高价氧化物的化学式为SeO3
C.硒的非金属性比溴弱
D.硒单质在空气中燃烧可生成二氧化硒
查看答案和解析>>
科目: 来源: 题型:
Na2CO3和NaHCO3的混合物2.74 g溶于水配成100 mL溶液,其中c(Na+)=0.4 mol·L-1,求:
(1)溶液中Na+的物质的量是多少?
(2)加热灼烧后剩余固体的质量是多少?
查看答案和解析>>
科目: 来源: 题型:
下图为周期表中原子体积(单质原子的摩尔体积)随原子
序数变化的关系。
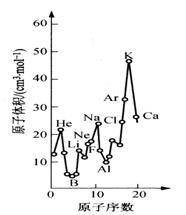 (1)第二周期原子体积最大的元素形成的固态单质属于
(1)第二周期原子体积最大的元素形成的固态单质属于
_________________晶体。第三周期原子体积最小的
元素核外电子排布式为________________________。
(2)试预测下列元素原子体积的关系:Se _____ Br;
Xe _____ Ba(选填 >、 = 或 < )。
(3)从图中可以得出的结论有__________(选填代号)。
a. 同一周期中,原子体积先由大变小,而后又
由小变大
b. 同周期金属元素中,碱金属的原子体积最大
c. 同一主族中从上到下,原子体积一般总是逐
渐减小
(4)由此可见,在元素周期表中,元素性质与它们
所形成的单质和化合物的性质均有周期性变
化规律。试写出一条ⅦA族元素所形成的化
合物某种性质的变化规律:
_____________________________。
查看答案和解析>>
科目: 来源: 题型:
 最近罗马大学Fulvio Cacace等人获得了极具理论研究意义的N4分子,N4分子结构如右图所示(与白磷P4相同)。已知断裂1mol N—N吸收167kJ热量,生成1mol
最近罗马大学Fulvio Cacace等人获得了极具理论研究意义的N4分子,N4分子结构如右图所示(与白磷P4相同)。已知断裂1mol N—N吸收167kJ热量,生成1mol ![]() 放出942kJ热量。由此判断下列说法正确的是
放出942kJ热量。由此判断下列说法正确的是
A.N4属于一种新型的化合物 B.N4与N2互为同素异形体
C.N4沸点比P4(白磷)高 D.1molN4气体转变为N2将放出882kJ热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com