
科目: 来源: 题型:
下列反应的离子方程式错误的是( )
A.向碳酸氢钙溶液中加人过量氢氧化钠Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-
B.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合
Ba2++2OH-+NH4++HCO3-==BaCO3↓+NH3·H2O+H2O
C.氢氧化铝与足量盐酸反应: Al(OH)3+3H+==Al3++3H2O
D.过量CO2通入氢氧化钠溶液中: CO2+2OH-==CO32-+H2O
查看答案和解析>>
科目: 来源: 题型:
下列有关胶体和溶液![]() 的比较中,正确的是( )
的比较中,正确的是( )
A.溶液中溶质粒子不带电,胶体分散质粒子带电
B.溶液中溶质的粒子运动有规律,胶体粒子运动无规律
C.通直流电后,溶液中溶质的粒子分别向两极运动,而胶体中分散质粒子向某一极运动
D.溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现光亮的“通路”
查看答案和解析>>
科目: 来源: 题型:
2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
![]()
![]() (1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
![]()
![]() (2)图中△H= KJ·mol-1;
(2)图中△H= KJ·mol-1;
![]()
![]() (3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式 ;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式 ;
![]()
![]() (4)如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)= mol·L-1·min-1、υ(SO3)= mol·L-1·min-1;
(4)如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)= mol·L-1·min-1、υ(SO3)= mol·L-1·min-1;
![]()
![]() (5)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H (要求计算过程)。
(5)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H (要求计算过程)。
查看答案和解析>>
科目: 来源: 题型:
下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
用化学符号回答下列问题:
(1)在这些元素中,最活泼的金属元素是 ,最活泼的非金属元素是 ,化学性质最不活泼的是: 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的是____ _ __,碱性最强的化合物的是:____ _____ ____。
(3)最高价氧化物是两性氧化物的元素是_____ ____;写出它的氧化物与氢氧化钠反应的离子方程式_____ _________ _________ _________ _________ ____。
(4)在这些元素中,原子半径最小的是 ,原子半径最大的是 。
(5)表示①与⑧的化合物的分子式 ,该化合物是由 (填“极性”“非极性”下同)键形成的。
(6)用电子式表示元素④与⑦的化合物的形成过程: ,该化合物属于 (填 “共价”或“离子”)化合物。
查看答案和解析>>
科目: 来源: 题型:
(分)(1)在硫酸铜晶体里结晶水含量的测定实验中,称量操作至少要进行 次。
(2)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、 、 。
(3)下面是中学化学中常用玻璃仪器组成的实验装置图(根据需要可在其中加入液体或固体)。

请回答下列问题:
①能用作干燥氨气的装置有_______________(填字母);
②既能用于收集氯气又能用于收集一氧化氮气体的装置有_______________(填字母);
③在实验室制备氯气的实验中,用以除去氯气中氯化氢等杂质气体的装置有________________ (填字母);
④能用于乙烯与溴水反应制二溴乙烷的实验装置有___________________(填字母);
⑤在C装置中,若用烧杯内的氢氧化钠溶液吸收尾气二氧化硫,则广口瓶的作用是___________________。
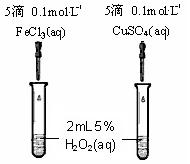 (4)为比较Fe3+和Cu2+对H2O2分解的催化效果,某同学设计了右图所示的实验。
(4)为比较Fe3+和Cu2+对H2O2分解的催化效果,某同学设计了右图所示的实验。
①可通过观察 来定性的得出结论;
②有A同学提出将CuSO4改为CuCl2更为合理,其理是 ;
若不采用A同学的改进方案,你认为还可以如何改 进? 。
查看答案和解析>>
科目: 来源: 题型:
将稀硝酸与稀氨水混合,不可能出现的结果是 ( )
A.pH=7,且c(NH4+)=c(NO3-)>c(H+)=c(OH-)
B.pH<7,且c(NO3-)+c(OH-)=c(H+)+c(NH4+)
C.pH<7,且c(H+)>c(NO3-)>c(OH-)>c(NH4+)
D.pH>7,且c(NH4+)>c(OH-)>c(NO3-)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
用下图装置可以进行测定SO2转化成SO3的转化率的实验。已知SO3的熔点是16.8℃,沸点是445.8℃。已知发生装置中所涉及反应的化学方程式为:
Na2SO3(s) + H2SO4(98%)==Na2SO4 + H2O + SO2↑
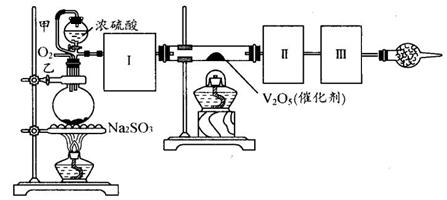
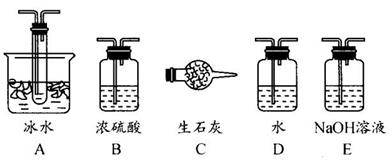
(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~E装置中选择最适合装置并将其序号填入下面的空格中。
Ⅰ、Ⅱ、Ⅲ处连接的装置分别是_______________、_______________、_______________。
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,应采取的操作是 。
(3)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式
(4)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为 %(用含a、b的代数式填写)
(5)尾端球形干燥管的作用是 。
查看答案和解析>>
科目: 来源: 题型:
下列排列顺序完全正确的有
①溶解性:Na2CO3>NaHCO3>AgCl>AgI;
②固体的热稳定性:Na2CO3>CaCO3>NaHCO3;
③氧化性:MnO2>Cl2>Fe3+>Cu2+;
④微粒半径:Fe(OH)3胶粒>K+>C1―>Na+;
⑤给出质子的能力:CH3COOH>C2H5OH>H2O
A.4项 B.3项 C.2项 D.1项
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com