
科目: 来源: 题型:
下列有关原子结构和元素周期律的表述正确的是( )
①原子序数为15的元素的最高化合价为+5
②ⅦA族元素是非金属性最强的元素
③第三周期ⅦA族元素的原子核电荷数和中子数不一定都为17
④原子序数为14的元素位于元素周期表的第三周期ⅥA族
A.①② B.①③ C.②④ D.③④
查看答案和解析>>
科目: 来源: 题型:
某盐的化学式XmYn为最简结构(m≠n),将一定量的盐溶于足量水时:
(1)若测得溶液的pH为5,则该盐与水反应的离子方程式可能为:__________________。
(2)若测得该盐溶液的pH为9,则该盐与水反应的离子方程式可能为:_______________。
(3)若X、Y为同周期的短周期元素,XmYn溶于水时,有白色沉淀产生,又有无色气体放出,则XmYn溶于水的化学方程式为:______________________________。
查看答案和解析>>
科目: 来源: 题型:
下列混合液中,各离子浓度的大小顺序正确的是()
A.10mL0.1mol·L-1NH4Cl溶液与5mL0.2mol·L-1NaOH溶液混合,c(Na+)>c(Cl-)>c(OH-)>c(H+)
B.10mL0.1mol·L-1氨水与10mL0.1mol·L-1盐酸混合,c(Cl-)>c(NH![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
C.10mL0.1mol·L-1CH3COOH溶液与5mL0.2moL·L-1NaOH溶液混合,c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.10mL0.5mol·L-1CH3COONa溶液与6mL1mol·L-1盐酸混合,c(Cl-)>c(Na+)>c(OH-)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
物质的量浓度相同时,下列既能跟NaOH溶液反应,又能跟盐酸溶液反应的溶液中,pH最大的是( )
A.Na2CO3溶液 B.NH4HCO3溶液
C.NaHCO3溶液 D.NaHSO4溶液
查看答案和解析>>
科目: 来源: 题型:
实验室在配制硫酸铁溶液时,先把硫酸铁晶体溶解在稀硫酸中,再加水稀释到所需的浓度,这样操作的目的是( )
A.提高硫酸铁的溶解度 B.防止硫酸铁分解
C.降低溶液的pH D.抑制硫酸铁水解
查看答案和解析>>
科目: 来源: 题型:
下列说法中,不正确的是( )
A.在NaAlO2溶液中,![]() 不可能大量存在
不可能大量存在
B.在0.1 mol·L-1的氢溴酸中加入适量的蒸馏水,溶液的c(H+)减小
C.在由水电离出的c(OH-)=1×10-12 mol·L-1的溶液中,Al3+不可能大量存在
D.室温下pH=6的酸性溶液中,可能存在NH3·H2O分子
查看答案和解析>>
科目: 来源: 题型:
在热的稀硫酸溶液中溶解了11.4 g FeSO4。当加入50 mL 0.5 mol·L-1 KNO3溶液后,使其中的Fe2+全部转化为Fe3+。KNO3溶液也完全反应,并有NxOy气体逸出,则该NxOy是
( )
A.N2O B.NO C.N2O3 D.NO2
查看答案和解析>>
科目: 来源: 题型:
![]() 在某一容积为5 L的密闭容器内,加入0.2 mol的CO和0.2 mol的H2O,在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g);ΔH>0。
在某一容积为5 L的密闭容器内,加入0.2 mol的CO和0.2 mol的H2O,在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g);ΔH>0。
反应中CO2的浓度随时间变化情况如下图:
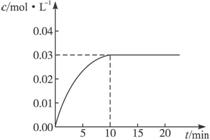
(1)根据上图数据,反应开始至达到平衡时,CO的化学反应速率为___________;反应达平衡时,c(H2)=______________。
(2)判断该反应达到平衡的依据是_________。
①CO减少的化学反应速率和CO2减少的化学反应速率相等
②CO、H2O、CO2、H2的浓度都相等k+s-5#u ![]()
③CO、H2O、CO2、H2的浓度都不再发生变化
④正、逆反应速率都为零
(3)如要一开始加入0.1 mol的CO、0.1 mol的H2O、0.1 mol的CO2和0.1 mol的H2,在相同的条件下,反应达平衡时,c(H2O)=_________。
查看答案和解析>>
科目: 来源: 题型:
莫尔盐[(NH4)2Fe(SO4)2·6H2O]常作氧化还原滴定法的基准物质,在0.1mol/L的该盐的溶液中,下列有关比较不正确的是( )
A.c(SO![]() )> c(NH
)> c(NH![]() )>c(Fe2+)>c(H+)>c(OH-)
)>c(Fe2+)>c(H+)>c(OH-)
B.c(NH3·H2O)+c(NH![]() )= 0.2mol/L
)= 0.2mol/L
C.c(H+)= c(OH-)+c(NH3·H2O)
D.2 c(SO![]() )+ c(OH-)= c(NH
)+ c(OH-)= c(NH![]() )+2 c(Fe2+)+c(H+)
)+2 c(Fe2+)+c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com