
科目: 来源: 题型:
下表是元素周期表的一部分,表中所列字母分别代表某一化学元素。

(1)i是铁元素,其原子的最外层电子数为2,请写出铁元素的原子结构示意图___________。
(2)由以上元素形成的金属单质中,熔点最低的是___________________。
(3)NH3·H2O的电离方程式为NH3·H2O![]()
![]() +OH-,试判断NH3溶于水后,形成的NH3·H2O的合理结构是______________________。
+OH-,试判断NH3溶于水后,形成的NH3·H2O的合理结构是______________________。

(4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是_________________________。(填写字母)
(5)利用稀有气体化合物,人们实现了许多制备实验上的突破。如用XeO3在碱性条件下与NaBrO3反应生成NaBrO4,同时放出Xe。写出上述反应方程式:_____________________。
查看答案和解析>>
科目: 来源: 题型:
图4-39是用石墨和铁作电极电解饱和食盐水的装置。请填空:
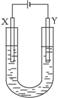
图4-39
(1)X的电极名称是_________极,发生的电极反应式为________,Y极的电极材料是_______。检验X极的产物方法是_____________________。
(2)某同学在实验时误将两种电极材料接反,导致X极上未收到预期产物。一段时间后又将两极的连接方式纠正过来,发现X一端出现了白色沉淀,此沉淀是_______(填化学式)。其形成原因是___________,该沉淀在空气中放置,现象是________________________。
(3)工业上电解饱和食盐水的方法之一,是将两个极室用离子交换膜隔开(如图4-40)其目的是_______,阳极室(A处)加入_______,阴极室(B处)加入_______,离子交换膜只许_________离子通过。

图4-40
查看答案和解析>>
科目: 来源: 题型:
在指定条件下一定能大量共存的离子组是( )
A、由水电离出的[OH-]=1×10-13mol/L的溶液中:Fe2+、NH4+、ClO-、Cl-
B、加入铝粉能放出氢气的溶液中:CO32-、AlO2-、I-、Na+
C、能使蓝色石蕊试纸变红色的溶液中:Fe2+、NO3-、SCN-、SO42-
D、加入酚酞试液,呈无色的溶液中:NH4+、K+、SO42-、Al3+
查看答案和解析>>
科目: 来源: 题型:
常温常压下,充分燃烧一定量的甲烷放出热量222.575KJ,经测定完全吸收生成的二氧化碳需消耗1mol/L的NaOH溶液250mL,恰好生成正盐。则此条件下甲烷的燃烧热热化学方程式 ( )
A.CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-890.3 kJ/mol
B. 1/2CH4(g)+O2(g)=1/2CO2(g)+H2O(l);△H=-222.575 kJ/mol
C. 1/2CH4(g)+O2(g)=1/2CO2(g)+H2O(g);△H=-445.15 kJ/mol
D. CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890.3 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
某校课外实验小组进行铜与浓、稀硝酸反应的实验研究。基本原则是:安全可靠、现象明显,符合环保要求。

如果用图Ⅰ中装置进行铜与浓硝酸反应的实验,最大缺点是产生的NO2气体逸出污染空气;如果用该装置来证明铜与稀硝酸反应生成NO气体,缺点是不易观察到有毒性的NO气体无色的本来面目。
(1)若用装置Ⅱ进行实验,既可克服实验不足,还能使上述反应在同一试管中连续进行。实验如下:组装好装置并检查气密性后,加入2 mL浓硝酸(铜片未接触酸液),塞紧胶塞;向左倾斜试管使其反应发生,当导管口有极少量红棕色气体逸出,溶液呈绿色时,正立试管,使反应停止;同时将导管插入水中,稍后能观察到:a.水沿导管倒吸至试管中,b.________________,c. ________________等明显现象。其中发生的原因用方程式表示为:_________________________________________________________。
(2)当试管中液体体积约占1/2时,从水中取出导管,并伸入一小试管中,管口塞上浸有碱液的棉花(如图Ⅲ)。这样做的目的是:________________,此时大试管中反应的离子方程式为:________________________________________________。
(3)若用右上图Ⅳ所示的装置(U形管、干燥管、A为活塞)制取NO可能更加理想。请补充下列实验步骤:
①检查装置的气密性的方法是:________________________________________________。
②打开活塞A,从U形管右端注入稀硝酸,直到________________________为止。
③关闭活塞A,若反应缓慢,可在U形管左侧加热,观察到____________________。
查看答案和解析>>
科目: 来源: 题型:阅读理解
2009年8月,陕西省凤翔县长青镇马道口村和邻村孙家南头村的村民们自发到宝鸡各大医院检测发现,两村数百名婴幼儿及儿童绝大多数被检测出体内铅含量超标,其中部分超标严重,已达到中毒标准。两村民居南北环抱着的一家年产铅锌20万吨的冶炼企业,被疑与此有关。
(1)铅(原子序数为82)位于元素周期表的 周期 族,已知+2价铅比+4价铅稳定,+4价铅有较强的氧化性。将PbO2与浓盐酸加热反应产生黄绿色的气体,写出该反应的离子方程式 ,将SO2通入棕色PbO2的悬浊液中会产生白色沉淀,写出该反应的化学方程式 。
(2)铅锭冶炼厂采用火法冶炼铅,铅在自然界中以方铅矿(PbS)的形式存在,主要生产过程是先煅烧方铅矿制成PbO,再用CO还原PbO制备铅。上述生产过程中的主要化学方程式为 、 。
(3)铅蓄电池是典型的可充电型电池,它的正负极板是惰性材料,电池总反应式为:
![]() 。放电时正极的电极反应式是 ;电解液中H2SO4的浓度将(填“变大”“变小”或“不变“);当外电路通过电子2mol时,理论上负极板的质量增加 g。
。放电时正极的电极反应式是 ;电解液中H2SO4的浓度将(填“变大”“变小”或“不变“);当外电路通过电子2mol时,理论上负极板的质量增加 g。
(4)铅在工业中应用广泛,如为了增强彩釉的亮度,陶瓷业在釉中常加入少量的铅。铅在酸性溶液中容易溶解,生成+2价铅进入人体,写出铅“吃醋”的化学方程式: 。汽车工业为提高发动机的使用寿命,常在汽油中加入抗震剂四乙基铅的分子式: 。
查看答案和解析>>
科目: 来源: 题型:
用饱和的氯化铁溶液制取氢氧化铁胶体,正确的操作是( )
A.将FeCl3溶液滴入蒸馏水中即可
B.将FeCl3溶液滴入热水中,得到黄色液体即可
C.将FeCl3溶液滴入沸水中,得到红褐色溶液即可
D.将FeCl3溶液滴入沸水中,并继续加热煮沸至生成红褐色沉淀即可
查看答案和解析>>
科目: 来源: 题型:
将二氧化硫通到滴有酚酞的NaOH试液中,发现红色消失。主要原因是
A.二氧化硫有漂白性 B.二氧化硫有还原性
C.二氧化硫有氧化性 D.二氧化硫溶于水后,溶液显酸性
查看答案和解析>>
科目: 来源: 题型:
下列应用技术与胶体分散系性质有关的是( )
①利用电泳分离蛋白质 ②电泳用于汽车外壳的涂漆 ③医用微波手术刀,利用其在进行手术时所发生的微波,加热“割口”附近血液中的蛋白质使血液凝固,减少流血量 ④加明矾使江水变澄清
A.①②③④ B.③④ C.①④ D.②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com