
科目: 来源: 题型:
下列各溶液中pH最大的是( )
A.pH=4的醋酸和pH=10的烧碱溶液等体积混合
B.pH=5的盐酸稀释100倍
C.pH=9的烧碱溶液稀释100倍
D.pH=9的氨水稀释100倍
查看答案和解析>>
科目: 来源: 题型:
![]()
![]()
![]() (09全国卷)
(09全国卷)![]()
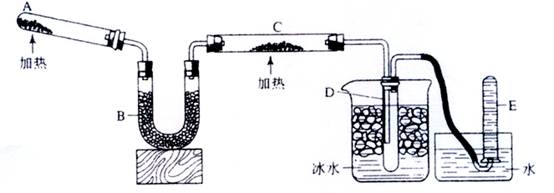
![]() 已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
![]()
![]()
![]()
![]()
![]()
![]() 回答下列问题:
回答下列问题:
![]()
![]() (1)A中加入的物质是_______.
(1)A中加入的物质是_______.![]()
![]() 发生反应的化学方程式是____________;
发生反应的化学方程式是____________;
![]()
![]() (2)B中加入的物质是______,其作用是____________:
(2)B中加入的物质是______,其作用是____________:
![]()
![]() (3)实验时在C中观察到得现象是_______________,
(3)实验时在C中观察到得现象是_______________,![]()
![]() 发生反应的化学方程式是______________________;
发生反应的化学方程式是______________________;
![]()
![]() (4) 实验时在D中观察到得现象是___,
(4) 实验时在D中观察到得现象是___,![]()
![]() D中收集到的物质是____,检验该物质的方法和现象是____________.
D中收集到的物质是____,检验该物质的方法和现象是____________.
查看答案和解析>>
科目: 来源: 题型:
能影响水的电离平衡,并使溶液中的C(H+)>C(OH-)的措施是 ( )
A.向纯水中投入一小块金属钠 B.将水加热煮沸
C.向水中通入SO2 D.向水中加入NaCl
查看答案和解析>>
科目: 来源: 题型:
NO2存在于下列平衡:2NO2(g)![]() N2O4(g) △H<0。在测定NO2的相对分子质量时,下列条件较为适宜的是( )
N2O4(g) △H<0。在测定NO2的相对分子质量时,下列条件较为适宜的是( )
A.温度130℃,压强3.03×105Pa B.温度25℃,压强1.01×105Pa
C.温度130℃,压强5.05×104Pa D.温度25℃,压强5.05×104Pa
查看答案和解析>>
科目: 来源: 题型:
下列事实中,不能用勒夏特列原理来解释的是( )
A.加入催化剂有利于氨氧化反应
B.使氢硫酸中加碱有利于S2-离子增多
C.500℃左右比室温更有利于合成氨反应
D.高压条件有利于合成氨
查看答案和解析>>
科目: 来源: 题型:
某温度下,在密闭容器中进行SO2的催化氧化反应。若起始时[SO2]=[O2]=6mol/L,平衡时测得[O2]=4.5mol/L,则下列叙述中正确的是( )
A.SO2的转化率为60%
B.SO3的产率为50%
C.平衡时总压强与起始压强之比为7∶8
D.平衡时VSO2∶VO2∶VSO3=3∶3∶1
查看答案和解析>>
科目: 来源: 题型:
可以证明可逆反应N2 + 3H2![]() 2NH3已达到平衡状态的是:①一个N-N断裂的同时,
2NH3已达到平衡状态的是:①一个N-N断裂的同时,
有3个H-H键断裂;②一个N-N键断裂的同时,有6个N-H键断裂;③其它条件不变
时,混合气体平均式量不再改变;④保持其它条件不变时,体系压强不再改变;⑤NH3%、
N2%、H2%都不再改变;⑥恒温恒容时,密度保持不变;⑦正反应速率v(H2)=0.6mol/(L·min)
逆反应速率v(NH??3)=0.4mol/(L·min)。( )
A.全部 B.只有①③④⑤ C.②③④⑤⑦ D.只有①③⑤⑥⑦
查看答案和解析>>
科目: 来源: 题型:
下列事实不能用勒夏特列原理解释的是( )
A.煅烧粉碎的硫铁矿利于SO2的生成
B.对2HI(g) ![]() I2(g)+H2(g),增大压强可使平衡体系颜色变深
I2(g)+H2(g),增大压强可使平衡体系颜色变深
C.反应NO2+CO![]() CO2 +NO;ΔH<0,升高温度可使平衡向逆反应方向移动
CO2 +NO;ΔH<0,升高温度可使平衡向逆反应方向移动
D.合成NH3反应:N2+3H2![]() 2NH3 ΔH<0,为提高NH3的产率,理论上应采取降低温度的措施
2NH3 ΔH<0,为提高NH3的产率,理论上应采取降低温度的措施
查看答案和解析>>
科目: 来源: 题型:
向含0.02 mol Al3+的明矾溶液中逐滴加入0.2 mol·L-1的Ba(OH)2溶液时,测得产生沉淀的质量m和逐滴加入的Ba(OH)2溶液的体积V的关系如右图所示。
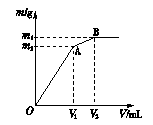
(1)写出两个阶段OA、AB反应的离子方程式。
OA段: ;
AB段: 。
(2)计算出A点、B点所对应的m、V以及沉淀的化学式,填在下面横线上。
V1= ,m1= ,沉淀的化学式 ;
V2= ,m2= ,沉淀的化学式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com