
科目: 来源: 题型:
(12分)2008年9月25日我国“神七”成功发射,标志着我国载人航天技术迈出重要的一步。“神七”以N2H4和N2O4燃料,N2H4学名为肼又称联氨,无色油状液体,具有与氨相似的气味,毒性很大。
⑴水电离成H3O+和OH-叫做水的自偶电离。同水一样,N2H4也有微弱的自偶电离,其自偶电离的方程式为: 。
⑵氨显碱性的原因在于NH3分子中的N原子具有孤对电子,它能通过配位键结合水中的H+,使水电离出OH-,其过程可以表示为NH3+H2O![]() NH4++OH-。试问N2H4与足量盐酸反应的化学方程式: 。
NH4++OH-。试问N2H4与足量盐酸反应的化学方程式: 。
⑶已知硼酸[B(OH)3]为一元弱酸,其显示酸性的原理与NH3、N2H4显示碱性的原理类似,试用离子方程式表示其显示酸性的过程: 。
⑷N2H4和N2O4反应温度达2700摄氏度,产生无污染的气体。1g 液态N2H4与足量的液态N2O4充分反应生成两种气态物质,可放出a KJ热量,试写出该反应的热化学方程式:
。
查看答案和解析>>
科目: 来源: 题型:
设某元素原子核内的质子数为m,中子数为n,则下述论断正确的是
A.不能由此确定该元素的相对原子质量
B.这种元素的相对原子质量为m+n
C.若碳原子质量为wg,此原子的质量为(m+n)wg
D.核内中子的总质量小于质子的总质量
查看答案和解析>>
科目: 来源: 题型:
作为国家正在实施的“西气东输”工程终点站——上海将逐步改变以煤、石油为主的能源结构,这对解决城市环境污染意义重大。目前上海大部分城市居民使用的燃料主要是管道煤气,浦东新区居民开始使用东海天然气作为民用燃料。管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4,它们的燃烧反应如下:
2CO+O2![]() 2CO2,2H2+O2
2CO2,2H2+O2![]() 2H2O,CH4+2O2
2H2O,CH4+2O2![]() CO2+2H2O
CO2+2H2O
根据以上反应的化学方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是__________;因此燃烧管道煤气的灶具如需改烧天然气,则灶具的改进方法是____________进风口(“增大”或“减小”),如不做改进可产生的不良结果是_____________________________。
管道煤气中含有的烃类除甲烷外还有少量的乙烷、丙烷、丁烷等。它们的某些性质见下表:
| 乙烷 | 丙烷 | 丁烷 | |
| 熔点/℃ | -183.3 | -189.7 | -138.4 |
| 沸点/℃ | -88.6 | -42.1 | -0.5 |
试根据以上某个关键数据解释冬天寒冷季节有时管道煤气火焰很小,并且呈断续状态的原因是____________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
A、B分别为第3周期和第4周期的同一主族的不同元素的原子,它们原子核内的质子数都等于中子数。
(1)若A为第ⅡA族元素原子,其质量数为x,B的质子数为y;
(2)若A为第ⅣA族元素原子,其质子数为m,B的质量数为n。
则y、n的值分别为( )
A.(x/2+18)和(2m+18) B.(x/2+8)和(2m+18)
C.(x/2+8)和(2m+36) D.(x/2+18)和(2m+36)
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E、F六种短周期元素的原子序数依次增大。A、D同族,B、C同周期;C是F不同周期的邻族元素;B原子最外层电子数是次外层的两倍;A、B两元素的核电荷数之差等于它们的原子最外层电子数之和;E和F的原子序数之和为30。由上述六种元素中的两种元素组成的甲、乙、丙、丁、戊、己六种化合物如下图所示:
| 化合物 | 甲 | 乙 | 丙 |
| 各元素原子个数比 | N(A)∶N(C)=2∶1 | N(A)∶N(C)=1∶1 | N(B)∶N(A)=1∶1 |
| 化合物 | 丁 | 戊 | 己 |
| 各元素原子个数比 | N(D)∶N(C)=1∶1 | N(E)∶N(F)=1∶3 | N(B)∶N(F)=1∶4 |
请完成下列问题:
(1)化合物己的电子式:__________________________。
(2)向含有1 mol乙的水溶液中加入MnO2,该反应中电子转移的物质的量为____________mol。
(3)化合物丙中所有的原子都在同一直线上,实验室制取丙的化学方程式为_______________。
(4)F的单质与甲反应的离子方程式为___________________________。
(5)将丁与二氧化碳反应生成的盐置于戊的水溶液中,发生反应的离子方程式为___________。
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是 ( )
A.Na2O2是碱性氧化物,能和水反应生成NaOH
B.Na在空气中的燃烧需要预先加热,所以该反应为吸热反应
C.NaHCO3不稳定,在一定条件下可以转化成Na2CO3
D.Na和盐不能发生置换反应
查看答案和解析>>
科目: 来源: 题型:
葡萄糖是人体所需能量的重要来源之一。葡萄糖燃烧的热化学方程式为:
C6H12O6(s)+6O2(g) ![]() 6CO2(g)+6H2O(l) ΔH=-2800kJ·mol-1葡萄糖在人体组织中氧化的热化学方程式与它燃烧的热化学方程式相同。计算100 g葡萄糖在人体中完全氧化时所产生的热量。?????????
6CO2(g)+6H2O(l) ΔH=-2800kJ·mol-1葡萄糖在人体组织中氧化的热化学方程式与它燃烧的热化学方程式相同。计算100 g葡萄糖在人体中完全氧化时所产生的热量。?????????
查看答案和解析>>
科目: 来源: 题型:
已知甲烷和一氧化碳的混合气体共0.75mol,完全燃烧后,生成二氧化碳气体和18g液态水,并放出515kJ的热量,若甲烷的燃烧热化学方程式为CH4(g)+2O2(g)![]() CO2(g)+2H2O(l);ΔH=-890kJ·mol-1,则CO气体燃烧的热化学方程式为_________。
CO2(g)+2H2O(l);ΔH=-890kJ·mol-1,则CO气体燃烧的热化学方程式为_________。
查看答案和解析>>
科目: 来源: 题型:
用铁片与稀硫酸反应制取H2时,下列措施不能使H2生成速率加大的是( )
A.对该反应体系加热 B.不用稀H2SO4,改用98%的浓H2SO4
C.滴加少量CuSO4 D.不用铁片,改用铁粉
查看答案和解析>>
科目: 来源: 题型:
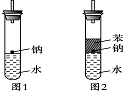
某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸 ②Na+水 ③Al+NaOH溶液。为点燃上述三个反应生成的H2,他们设计了如下装置(图1),请回答下列问题:
(1)写出Na与H2O反应的化学方程式_____________________________________。
(2)在点燃H2前必须先进行_____________________________________________,
方法是 _______________________________________________________。
 (3)实验小组在点燃用图1装置制得的H2时,①③实验获得成功,②却失败了。他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量太少。于是他们准备增加钠的用量,可老师说太危险,你认为产生危险的原因是________________________________________________________________________。
(3)实验小组在点燃用图1装置制得的H2时,①③实验获得成功,②却失败了。他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量太少。于是他们准备增加钠的用量,可老师说太危险,你认为产生危险的原因是________________________________________________________________________。
(4)实验小组查阅钠、苯、水的密度分别为0.97 g·mL-1、0.88 g·mL-1、1.00 g·mL-1,并据此对实验进行了改进(如图2),在改进后的实验中H2的生成速率减慢。原因是________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com