
科目: 来源: 题型:
下列离子方程式不正确的是
A.铝溶于NaOH溶液:2Al+OH-+2H2O ![]() 2AlO2- +3H2↑
2AlO2- +3H2↑
B.向强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:
3ClO-+2Fe(OH)3![]() 2FeO42 -+3Cl-+H2O+4H+
2FeO42 -+3Cl-+H2O+4H+
C.含Ca(HCO3)2的硬水中加入少量石灰水:Ca2++HCO3- +OH- ![]() CaCO3↓+H2O
CaCO3↓+H2O
D.碳酸氢钠溶液与硫酸氢钠溶液混合:H++HCO3- ![]() H2O+CO2↑
H2O+CO2↑
查看答案和解析>>
科目: 来源: 题型:
常温时,将500 ml pH=a的CuSO4 和K2SO4的混合溶液用石墨电极电解一段时间,测得溶液的pH变为b(假设溶液体积的变化忽略不计),在整个电解过程中始终发现只有一个电极有气体产生。下列说法错误的是( )
A..若使溶液恢复到电解前的浓度可以向溶液中加20(10-b-10-a)g CuCO3
B..b<a<7
C.阳极电极反应:2H2O—4e—=O2↑+4H+
D.整个过程中是阳极产生氧气,阴极析出铜单质
查看答案和解析>>
科目: 来源: 题型:
选择合适的序号填空
A.12C、13C 、14C B.S2-、Cl— 、Na+
C.金刚石、石墨、C60 D.Na+ 、Ne、F-
属于同素异形体的是 ,同位素的是 ,最外层电子数相同的微粒是 ,电子层数相同的微粒是 ,化学性质基本相同的是 。
查看答案和解析>>
科目: 来源: 题型:
E是某类化妆品生产的常用添加剂(香料),工业上以Y、X为主要原料合成,其中Y的产量可以用来衡量一个国家石油化工发展水平产品,其流程图如下。请完成填空:
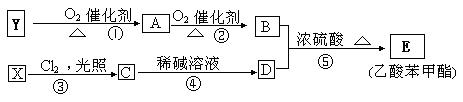
(1) 已知A、B的相对分子质量相差16,则A结构简式为 _
(2) 写出反应⑤的化学反应方程式
(3)E(乙酸苯甲酯)有多种同分异构体,其中属于酯类、且为一取代苯结构的有
种(不包括E本身),任写其中一种的结构简式 。
(4)除图示方法外,请你另设计一种最佳方案由Y制得A(用类似以上流程图表示)
(5)若将反应③、④的条件做如下变动,将先后得到![]() 、
、![]() 而得不到
而得不到![]() 、
、![]() :
:
![]()
已知![]() 与
与![]() 的分子式相同,且
的分子式相同,且![]() 可与
可与![]() 溶液发生显色反应,写出符合条件的由X→
溶液发生显色反应,写出符合条件的由X→![]() (
(![]() 的一硝基代物有2种)的反应方程式_______ 。
的一硝基代物有2种)的反应方程式_______ 。
查看答案和解析>>
科目: 来源: 题型:
标准状况下H2S和O2混合气体100mL,经点燃后反应至完全,所得气体经干燥后,恢复到原来状况时体积为10mL,该10mL气体可能是 ( )
![]() A.H2S、SO2 B.O2 C.H2S D.SO3
A.H2S、SO2 B.O2 C.H2S D.SO3
查看答案和解析>>
科目: 来源: 题型:
化合物A为一种常见金属元素与一种常见非金属元素组成的化合物,阳离子与阴离子的个数比为2:3。K为常见固态非金属单质,J为常见气态单质。其余为化合物,其中I、F在常温下为液态,C、D为刺激性气体,H无色无味气体,B为白色胶状沉淀,L为氯碱工业中的常见产品。F的浓溶液与K加热可生成D和H。(部分生成物未标出)

(1)写出H的电子式
(2)写出下列物质的化学式:
E J
(3)写出下列变化的化学方程式:
A + I → B + C
F的浓溶液与K加热可生成D和H
(4)写出下列变化的离子方程式:
B中加入L的水溶液
G的水溶液中通入过量的H
查看答案和解析>>
科目: 来源: 题型:
![]() 代表阿伏加德罗常数,下列叙述正确的是
代表阿伏加德罗常数,下列叙述正确的是
A.1mol/L Na2CO3溶液中的Na+数目为![]()
B.电解Na2CO3饱和溶液,若生成![]() 个H2,一定生成
个H2,一定生成![]() 个O2
个O2
C.常温常压下,46g NO2的原子数为![]()
D.1mol/L Na2O2与H2O完全反应时转移的电子数为![]()
查看答案和解析>>
科目: 来源: 题型:
用下图所示装置进行实验,表中叙述的结论不正确的是( )
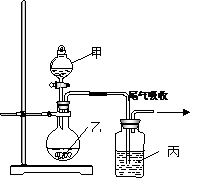
| 甲 | 乙 | 丙 | 结论 | |
| A | 盐酸 | 石灰石 | 苯酚钠溶液 | 酸性:HCl>H2CO3>苯酚 |
| B | 盐酸 | FeS | 溴水 | 还原性:S2->Cl->Br- |
| C | 浓盐酸 | KMnO4 | KBr溶液 | 氧化性:KMnO4>Cl2>Br2 |
| D | 水 | 电石 | 溴水 | 乙炔可与溴水反应 |
查看答案和解析>>
科目: 来源: 题型:
下列关于铜电极的叙述,正确的是 ( )
A.铜锌原电池中铜是正极
B.用电解法精炼粗铜时铜作阳极
C.在镀件上电镀铜时可用金属铜作阳极
D.电解稀硫酸制H2、O2时铜作阳极
查看答案和解析>>
科目: 来源: 题型:
铅蓄电池是化学电源,其电极材料分别是Pb和PbO2,电解质溶液为稀硫酸。工作时,该电池的总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O根据上述情况判断:
(1)蓄电池的负极是______,其电极反应式为______。
(2)蓄电池的正极是______,其电极反应式为______。
(3)蓄电池工作时,其中电解质溶液的pH______(增大、减小、不变)。
(4)实验室用铅蓄电池作电源电解饱和食盐水制取氯气,今若制得Cl2 0.050mol,这时电池内消耗的H2SO4的物质的量至少是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com