
科目: 来源: 题型:阅读理解
小明等同学为了探究酸、碱、盐溶液的导电性,设计了如下实验:
1.在5只250mL烧杯分别加入浓度均为0.1mol·L-1的盐酸、CH3COOH溶液、NaOH溶液、NaCl溶液、氨水各150mL。
2.在5种溶液中分别放入相同规格的石墨电极,按下图连接好。

3.接通电源,仔细观察现象。
现象1:五个灯泡都亮起来。
结论: 。
现象2:盐酸、氯化钠、氢氧化钠溶液对应的灯泡较亮,醋酸、氨水对应的灯泡较暗。
结论: 。
思考:
1.酸、碱、盐溶液导电与金属导电的原理是否相同,为什么?
2.同学们为了探究不同电解质之间电离能力的差异,设计了上述实验,通过观察灯泡的明亮程度,判断电解质的电离能力大小,为此必须控制其他能影响灯泡亮度的一些因素,使之保持一致,从而不影响灯泡的明亮程度。在本实验中,采取了哪些主要措施来控制其他因素对灯泡亮度的影响?(写出三条即可) 。
3.小明同学根据现象2得出一个结论:氯化氢、氯化钠、氢氧化钠是强电解质,醋酸、一水合氨是弱电解质。你同意他这个观点吗?为什么?
。
4.为了进一步探究氯化氢等化合物是强电解质,小红同学在老师的帮助下测定了0.1mol·L-1的盐酸中的氢离子浓度,通过对结果的分析,即可得出结论。说明氯化氢是强电解质的理由是:测得溶液中的氢离子浓度 0.1mol·L-1(选填>、<、=)。
5.同学们在实验的基础上,进一步查阅资料得知:一般来说, 是强电解质, 是弱电解质。根据以上结论推测:如果将上述实验中的醋酸和氨水混匀,然后分别盛放在原来的烧杯中。接通电源,可以观察到的现象是:
A.与混合前无任何区别。
B.5只灯泡都亮起来,亮度完全相同。
C.只有盐酸、氯化钠、氢氧化钠溶液对应的灯泡亮起来,另外两只不亮。
D.5个灯泡都亮起来,盐酸、氯化钠、氢氧化钠溶液对应的灯泡较亮,另外两只略暗,但明显比混合前明亮。
查看答案和解析>>
科目: 来源: 题型:
常温下,一种烷烃A和一种单烯烃B组成混合气体,A或B分子中最多只含有4个碳原子,且B分子的碳原子数比A分子的多。
⑴将1L该混合气体充分燃烧,在同温同压下得到2.5LCO2气体。试推断原混合气体中A和B所有可能的组合及其体积比,并将结果填入下表:
| 组合编号 | A的分子式 | B的分子式 | A、B的体积比 |
| ① | |||
| ② | |||
| ③ | |||
| ④ |
⑵120℃时取1L该混合气体与9LO2混合,充分燃烧,当恢复到120℃和原压强时,体积增大6.25%,试通过计算确定A、B的分子式。
查看答案和解析>>
科目: 来源: 题型:
某500 mL溶液中含0.1 mol Fe2+、0.2 mol Fe3+,加入0.2 mol铁粉,待Fe3+完全还原后,溶液中Fe2+的物质的量浓度为(假设反应前后体积不变)
A.0.4 mol / L B.0.6 mol / L C.0.8 mol / L D.1.0 mol / L
查看答案和解析>>
科目: 来源: 题型:
根据反应式①2Fe3++2I-=2Fe2++I2 ②Br2+2Fe2+=2Br-+2Fe3+可判断离子还原性由强到弱的顺序为
A.Br-、Fe2+、I- B.I-、Fe2+、Br-
C.Br-、I-、Fe2+ D.Fe2+、I-、Br-
查看答案和解析>>
科目: 来源: 题型:
有一种广泛应用于汽车、家电产品上的高分子涂料是按下列流程图生产的。
图中M(C3H4O)和A都可以发生银镜反应,N和M的分子中碳原子数相等,A的烃基上
一氯取代位置有三种。
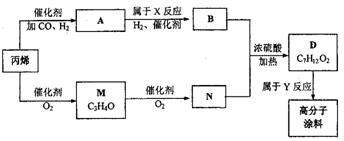
(1)试写出下列物质的结构简式:A M
(2)写出反应N+B![]() D的化学方程式:
D的化学方程式:
(3)写出反应类型:x ,Y
查看答案和解析>>
科目: 来源: 题型:
据悉,多哈亚运会上发令枪所用“火药”的主要成分是氯酸钾和红磷,撞击时发生化学反应:5KClO3+6P=3P2O5十5KCl 。下列有关该反应的叙述中,正确的是
A.反应中红磷是氧化剂
B.发令时产生的白烟全是KCl固体
C.反应中消耗3 mol P时,转移电子的物质的量为15 mol
D.“火药”中的红磷可以用白磷代替
查看答案和解析>>
科目: 来源: 题型:
图2-34是温度和压强对X+Y![]() 2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )

图2-34
A.上述可逆反应的正反应为放热反应
B.X、Y、Z均为气态
C.X和Y中只有一种为气态,Z为气态
D.上述反应的逆反应的ΔH>0
查看答案和解析>>
科目: 来源: 题型:
钢铁工业是国家工业的基础。2006年我国粗钢产量突破4亿t,居世界首位。某中学社会实践活动小组利用假期对当地钢铁厂进行了调研,对从矿石开始到钢铁产出的工艺流程有了全面的感性认识。请您对社会实践活动小组感兴趣的问题进行计算:
(1)将6.62g铁矿石样品投入适量的盐酸中(充分反应),过滤,然后在滤液中加过量的NaOH溶液,充分反应后,过滤、洗涤、灼烧得4.80g![]() 。现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00t生铁(含铁96%),至少需要这种铁矿石多少吨?(保留两位小数)
。现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00t生铁(含铁96%),至少需要这种铁矿石多少吨?(保留两位小数)
(2)取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到![]() 气体
气体
224mL。(标准状况)。
①计算此钢样粉末中铁和碳的物质的量之比。
②再取三份不同质量的钢样粉末分别加到l00mL相同浓度的![]() 。溶液中,充分反应后,测得的实验数据如下表所示:
。溶液中,充分反应后,测得的实验数据如下表所示:
| 实验序号 | I | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.812 | 5.624 | 8.436 |
| 生成气体的体积/L(标准状况) | 1.120 | 2.240 | 2.800 |
计算硫酸溶液的物质的量浓度。
③若在实验Ⅱ中继续加入mg钢样粉末,计算反应结束后剩余的固体质量为多少?(用含m的代数式表示)
查看答案和解析>>
科目: 来源: 题型:
一定条件下,向一带活塞的密闭容器中充入2 mol SO2和1 mol O2,发生下列反应:2SO2 (g)+O2 (g) 2SO3(g)。达到平衡后改变下列条件,SO3气体平衡浓度不改变的是( )
A.保持温度和容器体积不变,充入1 mol SO3 (g)
B.保持温度和容器内压强不变,充入1 mol SO3 (g)
C.保持温度和容器内压强不变,充入1 mol O2(g)
D.保持温度和容器内压强不变,充入1 mol Ar(g)
查看答案和解析>>
科目: 来源: 题型:
对某一可逆反应来说,使用催化剂的作用是( )
A.提高平衡的转化率 B.能同等程度地改变正、逆反应的速率
C.改变平衡混合物的组成 D.增大正反应的速率,减小逆反应的速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com