
科目: 来源: 题型:
能正确表示下列反应的例子方程式是
A.向次氯酸钙溶液通入过量CO2:Ca2++2ClO—+CO2+H2O =CaCO3↓+2HClO
B.向次氯酸钙溶液通入SO2:Ca2++2ClO—+SO2+H2O= CaSO3↓+2HClO
C.氢氧化钙溶液与碳酸氢镁溶液反应:HCO3—+Ca2++OH—=CaCO3↓+H2O
D.在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3—=3Fe3++NO↑+2H2O
查看答案和解析>>
科目: 来源: 题型:
某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量。实验步骤如下:
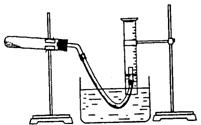 ①装好实验装置。②检查装置气密性。③把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为ag。
①装好实验装置。②检查装置气密性。③把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为ag。
④加热,开始反应,直到产生一定量的气体。
⑤停止加热(如图,导管出口高于液面)。
⑥测量收集到气体的体积。
⑦准确称量试管和残留物的质量为bg。
⑧测量实验室的温度。
⑨把残留物倒入指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净。
⑩处理实验数据,求出氧气的摩尔质量。
回答下列问题:
(1)如何检查装置的气密性?
(2)以下是测量收集到气体体积必须包括的几个步骤;①调整量简内外液面高度使之相同;②使试管和量筒内的气体都冷却至室温;③读取量筒内气体的体积。这三步操作的正确顺序是: (请填写步骤代号)。
(3)测量收集到气体体积时,如何使量筒内外液面的高度相同? 。
(4)如果实验中得到的氧气体积是c L(已换算成标准状况下),水蒸气的影响忽略不计,氧气的摩尔质量的计算式为(含a、b、c,不必化简):M(O2)= 。
查看答案和解析>>
科目: 来源: 题型:
x、y的原子序数均小于18,x原子K、L、M各电子层的电子数之比为1:4:1,它比y原子多3个电子,下列叙述正确的是( )
A.x离子半径大于y离子半径
B.y的单质与水反应可生成使带火星的木条复燃的气体
C.x原子半径大于y原子半径
D.x、y形成的化合物的摩尔质量为62
查看答案和解析>>
科目: 来源: 题型:阅读理解
某探究小组同学用金属铝分别与稀盐酸或稀硫酸反应的方法研究金属与不同酸反应的差异及影响反应速率的因素。
实验药品:2. 0moL/L盐酸、4. 0mol/L盐酸、2 .0mol/L硫酸、4.0mol/L硫酸,质量和相同的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50. 0mL,金属用量均为9. 0g。
(Ⅰ)甲同学用铝片分别和稀盐酸、稀硫酸反应,实验及其现象如下:
| 反应进程(分钟) | 1 | 2 | 5 | 15 | 20 |
| 4.0mol/L盐酸 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 反应结束 |
| 2.0mol/L硫酸 | 无明显现象 | 极少量气泡 | 少量气泡 | ||
| 4.0mol/L硫酸 | 无明显现象 | 少量气泡 | 有比较连续的气泡 | ||
请回答:
(1)写出铝与盐酸反应的离子方程式 。
(2)反应1~15min内,铝与盐酸的反应速率逐渐加快,其原因是
。
(3)以上探究铝与稀盐酸、稀硫酸反应速率有差异,你认为其原因有哪些可能?请提出你的假设(说出2种可能): 。
(Ⅱ)(1)乙同学设计了如下影响反应速率因素的实验(温度控制为25℃和35℃)。请你根据实验目的帮助该同学完成以下实验设计表(用量:酸均为50. 0mL、铝为9. 0g过量):
| 实验目的 | 实验 编号 | 温度 | 金属铝 形态 | 盐酸浓度 /mol??L-1 |
| 1. 实验①和②探究盐酸浓度对该反应速率的影响; 2. 实验①和③探究温度对该反应速率的影响; 3. 实验①和④探究金属规格(铝片、铝粉)对该反应速率的影响。 | ① | 25??C | 铝片 | 4. 0 |
| ② | ||||
| ③ | ||||
| ④ |
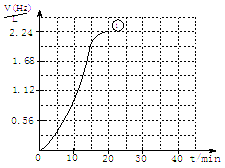 (2)右图为实验①的“H2—t”曲线图,若
(2)右图为实验①的“H2—t”曲线图,若
上述反应浓度减少一倍,速率是原来的1/2;温
度每升高10 ℃,反速率是原来的2倍。请在
答题卡的座标中画出实验②和实验③的“H2—t”
曲线图。
查看答案和解析>>
科目: 来源: 题型:
天然气的主要成分是甲烷。在某平衡体系中存在CH4、H2O、CO、H2四种气体,
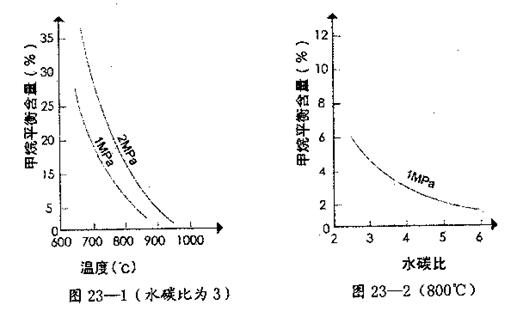
其平衡常数表达式为![]() 。已知温度、压强和水碳比[n(H2O)/n(CH4)]对甲烷转化反应的影响如下图:
。已知温度、压强和水碳比[n(H2O)/n(CH4)]对甲烷转化反应的影响如下图:
请回答下列问题:
(1)写出该可逆反应的化学方程式:
(2)根据图23—1判断△H 0,△S 0(选填“>”、“<”或“=”)。
(3)假设上述反应在恒容、恒温下进行,判断反应达到平衡状态时的标志是
A.CO减少的化学反应速率和H2O(曲减少的化学反应速率相等
B.CO、H2O(g)、CH4、H2的浓度都相等
C.CO、H20(g)、CH4、H2的浓度都不再发生变化
D.正、逆反应速率都为零
(4)在图23—2中画出压强为2 MPa时,CH4平衡含量与水碳比之间关系曲线。
查看答案和解析>>
科目: 来源: 题型:
关于非金属元素Cl、Si、S、N的叙述,正确的是 ( )
A.在通常情况下其单质均为气体
B.其单质均由双原子分子构成
C.都有相应的含氧酸
D.每种元素仪存在一种氧化物
查看答案和解析>>
科目: 来源: 题型:
工业生产中物质的循环利用有多种模式。例如:
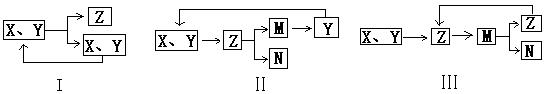 下列表述不正确的是
下列表述不正确的是
A.图I为合成氨,其中N2、H2循环使用
B.图Ⅱ为电解熔融MgCl2得到镁,其中HCl循环使用
C.图Ⅲ为氨氧化法制硝酸,其中NO循环使用
D.图I可用于侯氏制碱法制纯碱中CO2的循环
查看答案和解析>>
科目: 来源: 题型:
分类是学习和研究化学的一种常用的科学方法。下列分类合理的 ( )
①根据酸分子中含有的H原子个数将酸分为一元酸、二元酸
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素
④根据反应的热效应将化学反应分为放热反映和吸热反应
⑤根据分散系的稳定性大小将混合物分为胶体、溶液和浊液
A.只有②④ B.只有②③⑤ C.只有①②④ D.只有②③⑤
查看答案和解析>>
科目: 来源: 题型:
化学与生活密切相关,下列说法错误的是 ( )
A.“加铁酱油”可有效预防缺铁性贫血
B.维生素C具有还原性,在人体内起抗氧化作用
C.蛋白质水解产物氨基酸可以合成人体所需蛋白质
D.食品包装袋、食物保鲜膜等材料的主要成份是聚氯乙烯
查看答案和解析>>
科目: 来源: 题型:
现代科学研究的结果认为:煤是古代植物长期埋藏在地下处于空气不足的条件下,经历复杂的生物化学和物理化学变化逐渐形成的固体可燃矿物:石油是由远古海洋或湖泊中的生物在地下经过漫长的地球化学演化二形成的复杂混合物:天然气常常与石油伴生,煤、石油、天然气统称化石燃料。生物能是指从生物质(动物和植物)转化产生的一类能量,是一种无限的再生资源。通过以上材料分析:煤、石油、天然气和生物能资源的能量形成和转换利用过程基本上是( )
A.太阳辐射能→化学能热能 B 太阳辐射能→机械能→电能
C.生物能→电能→化学能→热能 D 太阳辐射能→机械能→化学能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com