
科目: 来源: 题型:
正确掌握好化学用语是学好化学的基础,下列有关表述正确物是 ( )
|
A.次氯酸的电子式:
B.质量数为16的氧原子的原子符号:816O
C.乙烯的结构简式:CH2CH2
D.亚硫酸氢根离子的电离方程式:![]()
查看答案和解析>>
科目: 来源: 题型:
某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol/L NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体 g。
(2)从图1中选择称量NaOH固体所需要的仪器是(填字母): 。
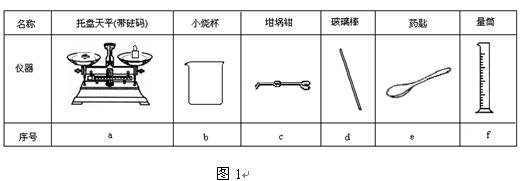
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图2所示。
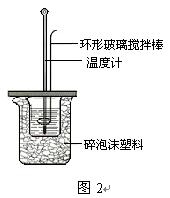
(3)写出该反应的热化学方程式(中和热为57.3 kJ/mol);
(4)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
| 温度 实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热△H= (取小数点后一位)。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母) 。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目: 来源: 题型:
一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2—。下列对燃料电池说法正确的是
A.在熔融电解质中,O2—由负极移向正极
B.电池的总反应是:2C4H10+13O2→8CO2+10H2O
C.通入空气的一极是正极,电极反应为:O2+4e—+2H2O=4OH—
D.通入丁烷的一极是正极,电极反应为:2C4H10+26e—+13O2—=4CO2+5H2O
查看答案和解析>>
科目: 来源: 题型:
由乙醛和乙酸乙酯组成的混合物中,若含碳的质量分数为A%,则此混合物中含氧的质量分数为( )
A.6A% B.(100-7A/6)% C.A/6% D.10A%
查看答案和解析>>
科目: 来源: 题型:
已知可逆反应:Fe(s) + CO2(g)![]() FeO(s) + CO(g),其温度与平衡常数K的关系如下表:
FeO(s) + CO(g),其温度与平衡常数K的关系如下表:
| T(K) | 938 | 1173 |
| K | 1.47 | 2.15 |
(1)写出该反应的平衡常数表达式____________________。
(2)若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,改变下列条件再达平衡后判断(选填“增大”、
“减小”、“不变”):
①升高温度,混合气体的平均相对分子质量_________;
②充入氦气,混合气体的密度__________。
(3)该反应的逆反应速率随时间变化情况如右图所示。
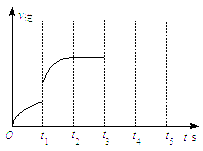
①从右图可知,在t1时改变了某种反应条件,反应在
t2时达到平衡,改变的条件可能是_______(选填编号)。
a.升高温度 b.增大CO2的浓度
c.减小CO2的浓度 d.使用催化剂
②如果在t3时增加CO2的量,t4时反应又处于新平衡状态,请在上图![]() 画出t3~ t5时间段的v逆变化曲线。
画出t3~ t5时间段的v逆变化曲线。
③能作为判断该反应达到平衡状态的依据是 (选填编号)。
a.v正(CO2)=v逆(CO) b.容器内气体总压强不再变化
c.容器内气体密度不再变化 d.使用催化剂后,正、逆反应速率同比例加快
查看答案和解析>>
科目: 来源: 题型:
下列有关实验的现象描述正确的是
A.氢气在氯气中燃烧,火焰呈苍白色,产生大量白雾
B.硫在空气中燃烧,发出明亮的蓝紫色火焰,产生有刺激性气味的气体
C.铜在氯气中燃烧,产生白烟,加水溶解后可能得到绿色溶液
D.用洁净的玻璃棒蘸取碳酸钾粉![]() 末在酒精灯火焰上灼烧,可观察到明亮的紫色火焰
末在酒精灯火焰上灼烧,可观察到明亮的紫色火焰
查看答案和解析>>
科目: 来源: 题型:
2008年诺贝尔化学奖授予美籍华裔钱永健等三位科学家,以表彰他们发现和研究了绿色荧光蛋白。荧光素是发光物质的基质,5-羧基荧光素(5-FAM)结构简式如右图所示,在碱性条件下有强烈的绿色荧光,广泛应用于荧光分析等。下列有关5-FAM说法不正确的是
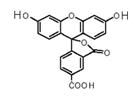
A.可与碳酸氢钠溶液反应
B.分子式为C21H12O7
C.1mol 该物质与足量NaOH溶液反应,可消耗4 mol氢氧化钠
D.不与FeCl3发生反应
查看答案和解析>>
科目: 来源: 题型:
在氢、氮、氯和钠四种元素中:
(1)有2种元素组成的共价化合物的水溶液显酸性,这种化合物的电子式是 ;
(2)有2种元素可形成离子化合物,用子电式表示其形成过程:
;
(3)在它们可能形成的双原子分子的单质中,化学性质最稳定的是:
。(写化学式)
查看答案和解析>>
科目: 来源: 题型:
已知X、Y、Z为三种由短周期元素构成的粒子,每摩粒子都有10mol电子,其结构特点如下:
| X | Y | Z | |
| 原子核数 | 单核 | 四核 | 双核 |
| 粒子的电荷数 | 1个单位正电荷 | 0 | 1个单位负电荷 |
现有A、B、C、D、E、F、G、H、I、J、K等物质,它们之间的相互反应转化关系如下图所示下图所示:
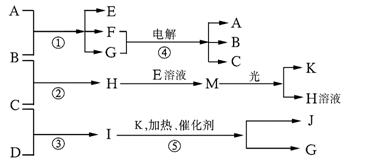
已知物质A由X、Z构成, B、C、D、K都是单质,G为无色液体,I的水溶液呈碱性,反应①~⑤都是用于工业生产的反应,请回答下列问题:?
(1) A的电子式为 ;D的结构式为 。
(2)物质B的组成元素在元素周期表中的位置是 。
(3)反应①的化学方程式为 。?
反应④离子方程式为 。?
(4)H和I反应的生成物的水溶液呈酸性,其原因是 (用一个离子反应方程式表示)
(5)已知每生成1mol I放出46.0kJ的热量,则反应③的热化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com