
科目: 来源: 题型:
下列物质中氧元素的化合价正确的是
A.H2O中氧元素的化合价为—l B.O2中氧元素的化合价为-2
C.NaOH中氧元素的化合价为—1 D.Na2O中氧元素的化合价为-2
查看答案和解析>>
科目: 来源: 题型:
实验室制取硝基苯常用如图装置。
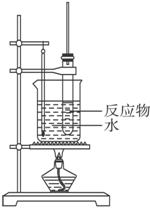
(1)苯的硝化反应是在浓H2SO4和浓HNO3的混合液中进行的,其中浓H2SO4的作用是_____________。
(2)在往试管中加入苯时为何要逐滴加入且不断振荡试管?
(3)温度计悬挂在烧杯中的水中,目的是________________________________。
(4)本实验用水浴加热而不直接用酒精灯加热试管,其优点是_____________。
(5)被水浴加热的试管口都要带一长导管,其作用是_____________。
(6)反应完毕后,如何从试管内混合物中分离出硝基苯?
查看答案和解析>>
科目: 来源: 题型:
工业上将苯的蒸气通过赤热的铁合成一种可作传热载体的化合物,该化合物分子中苯环上的一氯代物有3种,1 mol该化合物催化加氢时最多消耗6 mol氢气,判断这种化合物可能是( )
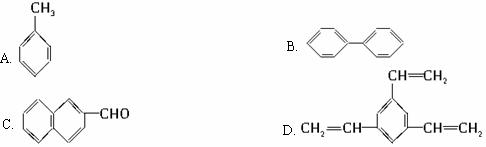
查看答案和解析>>
科目: 来源: 题型:
下列关于甲苯的实验中,能说明侧链对苯环有影响的是( )
A.甲苯硝化生成三硝基甲苯
B.甲苯能使酸性高锰酸钾溶液褪色
C.甲苯燃烧带有浓厚的黑烟
D.甲苯与氢气可以发生加成反应
查看答案和解析>>
科目: 来源: 题型:
实验室有甲、乙两瓶无色溶液,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液。为测定甲、乙两瓶溶液的成分及物质的量浓度,进行以下实验:
①量取25.00 mL甲溶液,向其中缓慢滴入乙溶液15.00 mL,共收集到224 mL(标准状况)气体。
②量取15.00 mL乙溶液,向其中缓慢滴入甲溶液25.00 mL,共收集到112 mL(标准状况)气体。
(1)判断:甲是________溶液,乙是_________溶液。
(2)实验②中所发生反应的离子方程式为_____________________________。
(3)甲溶液的物质的量浓度为 ,乙溶液的物质的量浓度为__________。
(4)将n mL甲溶液与等体积乙溶液按上述两种实验方式进行反应,所产生的气体的体积为V mL(标准状况),则V的取值范围是_____________________________。
查看答案和解析>>
科目: 来源: 题型:
用金属铂片插入KOH溶液中作电极,在两极上分别通入甲烷和氧气,形成甲烷—氧气燃料电池,该电池反应的离子方程式为:CH4+2O2+2OH-=CO32-+3H2O,试写出该电池的两极反应式。
查看答案和解析>>
科目: 来源: 题型:
(08年山东理综·29)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)=CH4(g)+HC![]() CH(g)+H2(g) △H1=156.6 kJ·mol-1
CH(g)+H2(g) △H1=156.6 kJ·mol-1
CH3CH![]() CH2(g)=CH4(g)+HC
CH2(g)=CH4(g)+HC![]() CH(g ) △H2=32.4 kJ·mol-1
CH(g ) △H2=32.4 kJ·mol-1
则相同条件下,反应C3H8(g)=CH3CH![]() CH2(g)+H2(g) 的△H= kJ·mol-1。
CH2(g)+H2(g) 的△H= kJ·mol-1。
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为 ;放电时CO32-移向电池的 (填“正”或“负”)极。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3![]() HCO3-+H+的平衡常数K1= 。(已知10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1= 。(已知10-5.60=2.5×10-6)
(4)常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液中c(H2CO3) c(CO32-)(填“>”、“=”或“<”),原因是 (用离子方程式和必要的文字说明)。
查看答案和解析>>
科目: 来源: 题型:
下列除去杂质的实验方法正确的是 …( )
A.除去CO中少量O2;通过灼热的Cu网后收集气体
B.除去K2CO3固体中少量NaHCO3;置于坩埚中加热
C.除去苯中溶有的少量苯酚;加入适量浓溴水反应后过滤
D.除去FeCl3酸性溶液中少量的FeCl2;加入稍过量双氧水后放置
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com