
科目: 来源: 题型:
1956年,杨振宁和李政道提出在弱相互作用中宇称不守恒,并由吴健雄用![]() 放射源进行了实验验证。次年,杨振宁、李政道两人因此获得诺贝尔物理奖。
放射源进行了实验验证。次年,杨振宁、李政道两人因此获得诺贝尔物理奖。![]() 的衰变方程为:
的衰变方程为:
![]() ====
====![]()
其中,Ve是反中微子,它的电荷为零,静止质量可认为是零。
(1)下列关于![]() 的叙述,错误的是_______________。
的叙述,错误的是_______________。
A.质子数是27 B.电子数是27
C.质量数是27 D.中子数是60
(2)CO与Fe同周期,它位于元素周期表的第_______________周期,第______________族。
(3)在上述衰变方程中,衰变产物Ni的质量数A为_______________,核电荷数Z为_______________。
(4)元素的化学性质主要决定于_______________。
A.核外电子数 B.核内质子数
C.核内中子数 D.最外层电子数
(5)不同种元素的本质区别是_______________。
A.质子数不同 B.中子数不同
C.电子数不同 D.质量数不同
查看答案和解析>>
科目: 来源: 题型:
有X、Y、Z三种溶液,在Na2CO3溶液中加入X,生成白色沉淀,在沉淀中加入Y,沉淀溶解并产生气体,再加入Z,又出现白色沉淀。X、Y、Z分别是( )
X Y Z
A.CaCl2 HNO3 KCl
B.BaCl2 HNO3 Na2SO4
C.KCl H2SO4 CaSO4
D.BaCl2 H2SO4 CaCl2
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z是3种短周期元素,其中X、Y位于同一族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的是
( )
A.元素非金属性由弱到强的顺序为Z<Y<X
B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4
C.3种元素的气态氢化物中,Z的气态氢化物最稳定
D.原子半径由大到小的顺序为Z>Y>X
查看答案和解析>>
科目: 来源: 题型:
多种氧化剂和多种还原剂共存时,存在“争先恐后,强者优先”现象。请理论预测,在含有Cu(NO![]() )
) ![]() 、Mg(NO
、Mg(NO![]() )
)![]() 和AgNO
和AgNO![]() 的溶液中加入适量锌粉,首先置换出来的是( )
的溶液中加入适量锌粉,首先置换出来的是( )
A.Mg B.Cu C.Ag D.H![]()
查看答案和解析>>
科目: 来源: 题型:
实验室制取乙烯的实验中:
(1)浓H2SO4的作用是_____________________________________________。
(2)浓H2SO4与酒精混合的操作是______________________________。
(3)迅速升温至170 ℃的原因是_____________________________________________。
(4)有效控制反应温度的方法是_____________________________________________。
(5)反应后一阶段的混合液体常变黑,并有刺激性气体生成,除去气体的方法是___________
_______________。
(6)在实验之前,首先应_______________,实验结束时,应先_______________。
查看答案和解析>>
科目: 来源: 题型:
相同温度时,下列两个反应的反应热分别用ΔH1 、ΔH2表示其关系正确的是( )
① H2(g)+ 1/2 O2(g)=H2O(g) ΔH1= -Q1kJ/mol
② 2H2O(l)=2H2(g)+ O2(g) ΔH2= +Q2kJ/mol
A. 2 Q1>Q2 B. Q1=Q2 C. 2Q1<Q2 D. 1/2 Q2=Q1
查看答案和解析>>
科目: 来源: 题型:
在一固定容积的反应器中发生反应:2SO2+O2![]() 2SO3,下列三种情况,其中开始反应时反应速率最快,达到平衡时,SO2的转化率最低的是( )
2SO3,下列三种情况,其中开始反应时反应速率最快,达到平衡时,SO2的转化率最低的是( )
①400 ℃,10 mol SO2和5 mol O2反应
②400 ℃,20 mol SO2和5 mol O2反应
③300 ℃,10 mol SO2和5 mol O2反应
A.① B.② C.③ D.无法判断
查看答案和解析>>
科目: 来源: 题型:
一定条件下,将SO2和O2充入一密闭容器中,发生如下反应:
2SO2(g)+O2(g)![]() 2SO3(g)(正反应放热)
2SO3(g)(正反应放热)
反应过程中SO2、O2、SO3物质的量变化如图2-61所示:
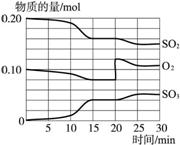
图2-61
完成下列问题:
(1)降低温度,SO2的转化率____________,化学反应速度____________。(填“增大”“减小”或“不变”)
(2)反应处于平衡状态的时间是____________。
(3)反应进行至20 min时,曲线发生变化的原因是________________________ (用文字表达)。10 min到15 min的曲线变化的原因可能是____________(填写编号)。
a.加了催化剂
b.缩小容器体积
c.降低温度
d.增加SO3的物质的量
查看答案和解析>>
科目: 来源: 题型:
电解原理在化学工业中有广泛的应用。如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X电极上的电极反应式为________。在X极附近观察到的现象是________。
②Y电极上的电极反应式为________,检验该电极反应产物的方法是________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是________,电极反应式为________________。
②Y电极的材料是________,电极反应式为________________(说明:杂质发生的电极反应不必写出)。
查看答案和解析>>
科目: 来源: 题型:
把15 g两种金属的混合粉未投入足量盐酸中,待反应完全后,得到11.2 L H2(标准状况下),下列各组中肯定不能组成上述混合物的是( )
A.Mg和Ag B.Cu和Zn C.Mg和Fe D.Al和Mg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com