
科目: 来源: 题型:
以下离子方程式均不正确,请改正。
(1)氧化铜与盐酸反应:O![]() +2H
+2H![]()
![]() H
H![]() O。正确的离子方程式是___________。
O。正确的离子方程式是___________。
(2)碳酸钡加入稀盐酸中:CO![]() +2H
+2H![]()
![]() CO
CO![]() ↑+H
↑+H![]() O。正确的离子方程式是___________________________________________________________________。
O。正确的离子方程式是___________________________________________________________________。
(3)铝粉加入硫酸铜溶液中:Cu![]() +Al
+Al![]() Cu+Al
Cu+Al![]() 。正确的离子方程式是________。
。正确的离子方程式是________。
(4)亚硫酸和氢氧化钡溶液混合:Ba![]() +SO
+SO![]()
![]() BaSO
BaSO![]() ↓。正确的离子方程式是__________________________________________________________________。
↓。正确的离子方程式是__________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
在周期表主族元素中,甲元素与乙、丙、丁三元素上下或左右紧密相邻。甲、乙两元素的原子序数之和等于丙元素的原子序数。这四种元素的最外层电子数之和为20。据此可以推断:
(1)元素甲为_______________,元素丙为_______________。
(2)元素乙和丁所形成化合物的化学式为_______________或_______________。
(3)四元素所形成的化合物相对分子质量最大的是_______________(写化学式),其分子内电子数为__________,它与水反应的化学方程式为__________(只写一个)。
查看答案和解析>>
科目: 来源: 题型:
在研究金属钠与氧气的反应时,将2.3 g金属钠在干燥的空气中氧化后,得到3.5 g固体,由此可判断其氧化产物为( )
A.只有Na2O2 B.只有Na2O
C.Na2O和Na2O2 D.无法确定
查看答案和解析>>
科目: 来源: 题型:
根据中学化学教材所附元素周期表判断,下列叙述不正确的是( )
A.K层电子为奇数的所有元素所在族的序数与该元素原子的K层电子数相等
B.L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
C.L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等
D.M层电子为奇数的所有主族元素所在族的序数与该元素原子M层电子数相等
查看答案和解析>>
科目: 来源: 题型:
根据Cu+2H![]() SO
SO![]() (浓)
(浓)![]() CuSO
CuSO![]() +SO
+SO![]() ↑+2H
↑+2H![]() O完成以下问题(已知Cu的相对原子质量为64):
O完成以下问题(已知Cu的相对原子质量为64):
(1)该反应中氧化剂是____________,被氧化的元素是______________。
(2)当有32 g Cu 溶解时,被还原的H![]() SO
SO![]() 的质量为___________g。
的质量为___________g。
查看答案和解析>>
科目: 来源: 题型:
已知 可简写为
可简写为![]() ,降冰片烯的分子结构可表示为
,降冰片烯的分子结构可表示为![]() 。
。
(1)降冰片烯属于_______________。
a.环烃 b.不饱和烃 c.烷烃 d.芳香烃
(2)降冰片烯的分子式为_______________。
(3)降冰片烯的一种同分异构体(含有一个六元环的单环化合物)的结构简式为___________
______________________________。
(4)降冰片烯不具有的性质______________________________。
A.能溶于水 B.能发生氧化反应
C.能发生加成反应 D.常温常压下为气体
查看答案和解析>>
科目: 来源: 题型:
在300 ℃时,5 L密闭容器内,分子式为A2和B2的两种气体反应,生成另一种气体C,其反应情况如图所示:则该反应的化学方程式为:__________________;A2的平均反应速率为_________。
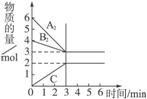
查看答案和解析>>
科目: 来源: 题型:
在密闭容器中,有一定起始浓度的氙(Xe)和F2反应,可得到3种氟化物。各种生成物在平衡体系内分压与反应温度的关系如图2-62所示(已知气体的分压之比等于物质的量之比)。
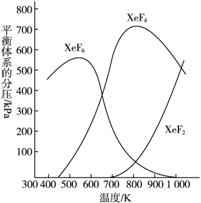
图2-62
(1)420 K时,发生反应的化学方程式为:___________________________;若反应中消耗1 mol Xe,则转移电子___________mol。
(2)600~800 K时,会发生反应:XeF6(g) ![]() XeF4(g)+F2(g),其反应热ΔH0(填“>”“=”或“<”=。理由是__________________________。
XeF4(g)+F2(g),其反应热ΔH0(填“>”“=”或“<”=。理由是__________________________。
(3)900 K时,容器中存在的组分有_____________________________。
查看答案和解析>>
科目: 来源: 题型:
NO和CO都是汽车尾气里的有害物质,它们能缓慢地起反应生成N2和CO2,下列对此反应的叙述正确的是( )
A.使用催化剂不能改变反应速率
B.降低压强能使反应速率加快
C.改变压强对反应速率没有影响
D.升高温度能加快反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com