
科目: 来源: 题型:
为了减少大气污染,许多城市推广清洁燃料。目前使用的清洁燃料主要有两类,一是压缩天然气(CNG),另一类是液化石油气。这两类燃料的主要成分是
A.碳水化合物 B.碳氢化合物 C.氢气 D.醇类
查看答案和解析>>
科目: 来源: 题型:
设计下列实验方案鉴别Na2CO3和NaHCO3两种白色粉末,不能达到预期目的的是
 |
A.分别向等量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢
B.分别向等量的白色粉末中加等体积适量的水,比较固体溶解量的多少
C.分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成
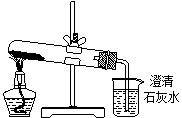
D.分别将等量的白色粉末用右图装置进行实验,比较澄清石灰水是否变混浊
查看答案和解析>>
科目: 来源: 题型:
(1)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:_________________________________。
(2)在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:_____________________。
查看答案和解析>>
科目: 来源: 题型:
Edward, you play so well. But I ______ you played the piano.
![]() A. didn’t know B. hadn’t known
A. didn’t know B. hadn’t known
![]() C. don’t know D. haven’t known
C. don’t know D. haven’t known
查看答案和解析>>
科目: 来源: 题型:
在氯化铵溶液中,下列关系式正确的是
A.c(Cl-)>c(NH![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.c(NH![]() )>c(Cl-)>c(H+)>c(OH-)
)>c(Cl-)>c(H+)>c(OH-)
C.c(Cl-)=c(NH![]() )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
D.c(NH![]() )=c(Cl-)>c(H+)>c(OH-)
)=c(Cl-)>c(H+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
下列说法,能够用勒沙特列原理来解释的是( )
A. 加入催化剂可以提高单位时间氨的产量
B. 高压有利于氨的合成反应
C. 500℃高温比室温更有利于合成氨的反应
D. 恒温恒容下,在合成氨平衡体系中充入He,使压强增大,则平衡正向移动,NH3增多
查看答案和解析>>
科目: 来源: 题型:
某化学课外小组用铜96%的废铜屑制取胆矾(五水合硫酸铜)。将铜屑放入稀硫酸中,加热并不断鼓入空气,在氧气作用下便生成硫酸铜。
(1)写出生成硫酸铜的化学方程式 。
(2)现用1 kg这种废铜屑理论上能制取胆矾多少千克?
(3)将胆矾与生石灰、水按质量比依次为1∶0.56∶100混合配制成无机铜杀菌剂波尔多液:
①此波尔多液中Cu2+离子和Ca2+离子的物质的量比为________(最简整数比)。
②波尔多液有效成分的化学式可表示为CuSO4·xCu(OH)2·yCa(OH)2,此种配比当x=1时,试确定y的数值________。
查看答案和解析>>
科目: 来源: 题型:
铁屑溶于过量的稀硫酸,过滤后向滤液中加入适量硝酸,再加入过量的氨水,有红褐色沉淀生成。过滤,加热沉淀物至质量不再发生变化,得到红棕色的残渣。上述沉淀和残渣分别为
A.Fe(OH)3;Fe2O3 B.Fe(OH)2;FeO
C.Fe(OH)2;Fe(OH)3;Fe3O4 D.Fe2O3;Fe(OH)3
查看答案和解析>>
科目: 来源: 题型:
对少量的碘化物可利用“化学放大”反应进行测定。其步骤如下:在中性或酸性介质中先用Br2将试样中的I-定量地氧化成碘酸盐,然后加入过量的KI,用CCl4萃取生成的I2(萃取率为100%)。分区水层后,用肼(即联氨H2N—NH2)的水溶液将I2反萃取至水层中(H2NNH2+2I2=4I-+N2+4H+),在用过量的Br2氧化,除去剩余的Br2后加入过量的KI,酸化,以淀粉作指示剂,用Na2S2O3标准溶液滴定(反应式为I2+2S2O32-=S4O62-+2I-),求得I-的含量。
(1)上述过程中有一些化学反应的方程式在题中未给出,请写出它们的离子方程式。
(2)根据有关反应的化学计量关系说明经上述步骤后试样中1molI-可消耗Na2S2O3的物质的量是多少?
(3)若在测定时,准确移取25.00mL含KI的试液,终点时耗用20.06mL0.100mol/L Na2S2O3溶液,请计算试液中KI的物质的量浓度。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com