
科目: 来源: 题型:
已知X、Y、Z元素的原子具有相同的电子层数,且原子序数依次增大,其最高价氧化物对应水化物酸性依次增强,则下列判断正确的是( )
A.原子半径按X、Y、Z的顺序增大 B.阴离子的还原性按X、Y、Z顺序增强
C.单质的氧化性按X、Y、Z顺序增强 D.氢化物的稳定性按X、Y、Z顺序增强
查看答案和解析>>
科目: 来源: 题型:
Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的离子与Ar原子的电子结构相同,且Y原子序数小于Z。
(1)Q的最高价氧化物,其固态属于 晶体,俗名叫 :
(2)R的氢化物分子的空间构型是 ,属于 分子(填“极性”或“非极性”);它与X形成的化合物可作为一种重要的陶瓷材料,其化学式为 ;
(3)X的常见氢化物的空间构型是 ,它的另一氢化物X2H4是火箭燃料的成分,其电子式是 ;
(4)Q分别与Y、Z形成的共价化合物的化学式是 和 ;Q与Y形成的化合物的电子式为 ,属于 分子(填“极性”或“非极性”)。
查看答案和解析>>
科目: 来源: 题型:
保持恒温、恒容,在某密闭容器中发生反应:2A(g)+2B(g)![]() C(g)+3D(g)。现分别从两条途径建立平衡:Ⅰ——从正反应开始,A、B的起始物质的量均为2mol ;Ⅱ——从逆反应开始,C、D的起始物质的量分别为2mol和6mol。以下叙述中正确的是
C(g)+3D(g)。现分别从两条途径建立平衡:Ⅰ——从正反应开始,A、B的起始物质的量均为2mol ;Ⅱ——从逆反应开始,C、D的起始物质的量分别为2mol和6mol。以下叙述中正确的是 ![]() 学科网
学科网
A.Ⅰ、Ⅱ两种途径从反应开始到平衡状态所消耗的时间相同![]() 学科网
学科网
B.Ⅰ、Ⅱ两种途径从反应开始到平衡状态的过程中,体系的总密度始终保持不变![]() 学科网
学科网
C.Ⅰ、Ⅱ两途径最终达到平衡时,体系内A的物质的量分数相同![]() 学科网
学科网
D.Ⅰ、Ⅱ两途径最终达到平衡时,体系内A的浓度相同![]() 学科网
学科网
查看答案和解析>>
科目: 来源: 题型:
(09广东卷)出土的锡青铜(铜锡合金)文物常有Cu2(OH)3Cl覆盖在其表面。下列说法正确的是
A.锡青铜的熔点比纯铜高
B.在自然环境中,锡青铜中的锡对铜起保护作用
C.锡青铜文物在潮湿环境中的腐蚀比干燥环境中快
D.生成Cu2(OH)3Cl覆盖物是电化学腐蚀过程,但不是化学反应过程
查看答案和解析>>
科目: 来源: 题型:
下列叙述中正确的是 ( )
A.任何化学反应都能设计成原电池;
B.任何氧化还原反应都能设计成原电池;
C.原电池反应一定是氧化还原反应
D.两个不同的金属电极用导线连接插入到电解质溶液中一定能形成原电池。
查看答案和解析>>
科目: 来源: 题型:
 早在1807年化学家戴维用电解熔融氢氧化钠制得钠, 4NaOH(熔)
早在1807年化学家戴维用电解熔融氢氧化钠制得钠, 4NaOH(熔) ![]() 4Na + O2↑+ 2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:
4Na + O2↑+ 2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:
3Fe+4NaOH![]() Fe3O4+2H2↑十4Na↑。下列有关说法正确的是
Fe3O4+2H2↑十4Na↑。下列有关说法正确的是
A.电解熔融氢氧化钠制钠,阳极发生电极反应为:
2OH--2e-=H2↑+O2↑
B.盖·吕萨克法制钠原理是利用铁的还原性比钠强
C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数也相同
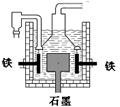
D.目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,
铁为阴极
查看答案和解析>>
科目: 来源: 题型:
智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘。
(1) 试配平该反应的化学方程式,并用短线标出电子转移方向及总数。
(2)
![]()
(2)已知含氧酸盐的氧化作用随溶液酸性的加强而增强,在制备实验时,定时取样,并用酸化的氯化钡来检测SO![]() 生成的量,发现开始阶段反应速率呈递增的趋势,试简述这一变化趋势发生的原因: 。
生成的量,发现开始阶段反应速率呈递增的趋势,试简述这一变化趋势发生的原因: 。
查看答案和解析>>
科目: 来源: 题型:
具有下列电子排布式的原子中,半径最大的是
A.1s22s22p63s23p1 B.1s22s22p1
C.1s22s22p3 D.1s22s22p63s23p4
查看答案和解析>>
科目: 来源: 题型:
实验室用铅蓄电池作电源电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:负极Pb+SO![]() ===PbSO4+2e-,正极PbO2+4H++SO
===PbSO4+2e-,正极PbO2+4H++SO![]() +2e-===PbSO4+2H2O今若制得Cl20.050 mol,这时电池内消耗的H2SO4的物质的量至少是
+2e-===PbSO4+2H2O今若制得Cl20.050 mol,这时电池内消耗的H2SO4的物质的量至少是
A.0.025 mol B.0.050 mol
C.0.10 mol D.0.20 mol
查看答案和解析>>
科目: 来源: 题型:
某烃A,相对分子质量为140,其中碳的质量分数为0.857。A分子中有两个碳原子不与氢直接相连。A在一定条件下氧化只生成G,G能使石蕊试液变红。
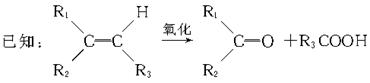
试写出:
(1)A的分子式 。
(2)与G同类的同分异构体(含G)可能有 种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com