
科目: 来源: 题型:
由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③
![]() 加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是( )
加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是( )
![]() A.②④⑤③① B.③②④①⑤ C.③④②⑤① D.②④③⑤①
A.②④⑤③① B.③②④①⑤ C.③④②⑤① D.②④③⑤①
查看答案和解析>>
科目: 来源: 题型:
下列对实验现象的预测或解释正确的是
A、向品红溶液中通入某无色气体,品红溶液退色,则该气体一定是二氧化硫
B、向血红色的硫氰化铁溶液中通入碘化氢气体,溶液不退色
C、向含酚酞的红色氢氧化钠溶液中通入无色的臭氧气体,红色可能退去
D、向碘化银的悬浊液中加入少量氯化银,并用力振荡,黄色变浅
查看答案和解析>>
科目: 来源: 题型:
A、B两种有机物均是有机合成的中间体,其中A的分子式为C4H7O2Br,B分子中含2个氧原子,其燃烧产物n(CO2) : n(H2O)=2:1,质谱图表明B的相对分子质量为188。A和B存在如下转化关系:

已知:①一个碳原子上连有两个羟基时,易发生下列转化:
![]()
② 同一个碳原子上连有两个双键的结构不稳定。请回答:
(1)C跟新制的氢氧化铜反应的化学方程式是 。
(2)A的结构简式是 。
(3)B的分子式是 。
(4)F具有如下特点:①具有弱酸性;②核磁共振氢谱中显示五种吸收峰;③苯环上的一氯代物只有两种;④除苯环外,不含有其他环状结构。写出符合上述条件的同分异构体有
种。
查看答案和解析>>
科目: 来源: 题型:
某实验小组设计用50 mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液进行中和反应,测定中和热,中和热测定实验的关键是要比较准确地配制一定物质的量浓度的溶液,量热器要尽量做到绝热;在量热的过程中要尽量避免热量的散失,比较准确地测量出反应前后溶液温度的变化。回答下列问题:
(1)中和热的测定所需的玻璃仪器有 。
(2)本实验中用稍过量的NaOH的原因是 。
(3)在反应中若因为有放热现象,而造成少量HCl挥发,则测得的中和热数值 (填偏高、偏低或不变)。
(4)该实验小组做了三次实验,每次取溶液各50mL,并记录如下原始数据。
| 实验序号 w. | 起始温度t1/℃ w.w.^w.k.&s.5*u.c.#om | 终止温度(t2)℃[来源:学科网ZXXK][来源:学。科。网] | 温差(t2-t1)℃[来源:Z+xx+k.Com] | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 w.w.^w.k.&s.5*u.c.#om | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 w.w.^w.k.&s.5*u.c.#om | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 w.w.^w.k.&s.5*u.c.#om | 31.9 w.w.^w.k.&s.5*u.c.#om | 6.8 |
已知盐酸、NaOH溶液密度近似为1.00g/cm3,中和后混和液的比热容 C=4.18J/(g·℃)则该反应的中和热为△H=_______________________________。
(5)若用等浓度的醋酸代替盐酸与NaOH溶液反应,则测得的中和热的数值会 (填偏高、偏低或不变),其原因 ![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应:3H2+N2![]() 2NH3 △H<0。反应过程中H2、N2和NH3物质的量变化如右图所示,据图判断下列叙述不正确的是
2NH3 △H<0。反应过程中H2、N2和NH3物质的量变化如右图所示,据图判断下列叙述不正确的是
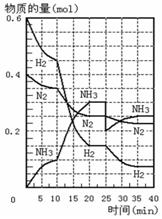
A.反应开始到第一次平衡时,N2的平均反应速率为0.0625 mol·(L·min)-1 ,H2的转化率为75%
B.反应达到第一次平衡时,反应的平衡常数表达式可写作:K=c2(NH3)/[ c3(H2) ·c(N2)]=(0.15 mol·L-1) 2/[ (0.075 mol·L-1) 3 ·(0.125 mol·L-1)]
C.从曲线变化可以看出,反应进行到10min至20min时可能采取的措施是使用了催化剂
D.从曲线变化可以看出,反应进行至25min时,采取的措施是分离出0.1mol的氨气,平衡正向移动
查看答案和解析>>
科目: 来源: 题型:
下列递变规律正确的是( )
A.HClO4、H2SO4、H3PO4的酸性依次增强 B.HCl、HBr、HI的稳定性依次增强
C.钠、镁、铝的还原性依次减弱 D.N、O、F原子半径逐渐增大
查看答案和解析>>
科目: 来源: 题型:
将 4 mol A 气体和 2 mol B 气体在 2 L 的密闭容器中混合并在一定条件下发生如下反应
2A(g)+B(g)![]() 2C(g);△H <0 4 s(秒)后反应达到平衡状态,此时测得 C 的浓度为0.6 mol·L-1 ,下列说法中正确的是
2C(g);△H <0 4 s(秒)后反应达到平衡状态,此时测得 C 的浓度为0.6 mol·L-1 ,下列说法中正确的是
A.反应过程中,当A 、B、C的物质的量浓度之比为 2:1:2时,反应即达到平衡状态
B.4 s 内用物质B表示的反应速率为0.075 mol·L-1·S-1
C.达平衡后若增大压强,A的转化率降低
D.达平衡后若升高温度,C的浓度将增大
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是:
A.由同种元素组成的物质一定是纯净物
B.在标准状况下,11.2 L NO与11.2 L O2混合后气体分子数为0.75NA
C.风化、石油分馏和碘的升华都是物理变化
D.1 mol C10H20ClBrO分子中共价键总数为32NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com