
科目: 来源: 题型:
下列说法正确的是 ( )
A.1 mol物质的质量叫做该物质的摩尔质量
B.两个等容容器,一个盛一氧化氮,另一个盛N2、H2混合气,同温同压下两容器内气体分子总数一定相同,原子总数也相同
C.将98 g H2SO4溶于500 mL水中所得到溶液中硫酸的物质的量浓度为2 mol/L
D.等物质的量的O2和O3其质量相等
查看答案和解析>>
科目: 来源: 题型:
现有下列实验用品:烧杯、铁架台(带铁圈)、三角架、分液漏斗、酒精灯、玻璃棒、 蒸发皿和蒸馏烧瓶,从缺少实验用品的角度分析,不能进行的实验项目是( )
A、过滤 B、蒸发 C、分液 D、萃取
查看答案和解析>>
科目: 来源: 题型:
磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性,制备时将含等物质的量的FeSO4和Fe2(SO4)3的溶液混合,再滴入稍过量的NaOH溶液,随后加入油酸钠溶液,即可生成黑色的、分散质粒子直径在55~36 nm的磁流体。下列说法中正确的是 ( )
A.所得的分散系属于悬浊液 B.该分散系能产生丁达尔效应
C.所得的分散系中分散质为Fe2O3 D.给分散系通直流电时,阳极周围黑色加深
查看答案和解析>>
科目: 来源: 题型:
土壤中有机物质含量的高低是判断土壤肥力的重要指标,通常通过测定土壤中碳的含量来换算。方法如下:
准确称量一定量的风干土样(m g),加入已知过量的K2Cr2O7酸性溶液煮沸,使土壤中的“碳”被氧化,反应的化学方程式为:2K2Cr2O7+3C+8H2SO4 ==== 2K2SO4+2Cr2(SO4)3+3CO2↑+8H2O;然后用FeSO4溶液(浓度为c mol·L-1)滴定剩余的K2Cr2O7,用去FeSO4溶液V1 mL。另取一份同量的K2Cr2O7酸性溶液,也用相同的FeSO4溶液滴定,用去V2 mL。
(1)写出FeSO4溶液和酸性K2Cr2O7溶液反应的离子方程式。
(2)若上述实验中m=2.0 g,c=0.2 mol·L-1, V1=19.50 mL,V2=42.60 mL;另知上述方法中只有96%的碳被氧化,且有机物质中碳的平均含量为58%。试计算上述土壤中有机物质的质量分数。
查看答案和解析>>
科目: 来源: 题型:
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
(1)冶炼铜的反应为8CuFeS2+21O2![]() 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
(2)上述冶炼过程中产生大量SO2。下列处理方案合理的是 (填代号)。
a.高空排放
b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO3
d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:S2O82-+2I-=2SO42-+I2
通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上
述反应的催化过程。 、
(不必配平)。
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、AI2O3)可制备Fe2O3。方法为
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得。
据以上信息回答下列问题:
a.除去Al3+的离子方程式是 。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为 。证明炉渣中含有的实验现象为
。
查看答案和解析>>
科目: 来源: 题型:
某同学用废干电池内的黑色固体(可能含有MnO2、NH4Cl、ZnCl2等物质)进行如图所示实验: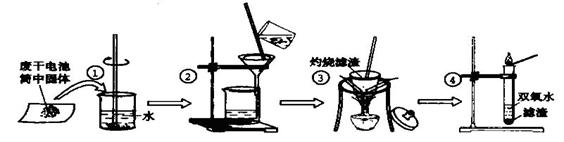
(1)操作②中过滤时玻璃棒的作用: ;
(2)操作④加入③中所得滤渣,试管中迅速产生能使带火星的木条复燃的气体,由此推测滤渣含有MnO2,试管中发生反应的化学方程式: ;
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中除含有MnO2外,还存在的物质为: 。
(4)已知氯化锌与稀氨水反应先生成Zn(OH)2白色沉淀,Zn(OH)2可以溶于稀氨水生成可溶性的Zn(NH3)4(OH)2;下列是该同学对操作②的滤液主次成分进行探究的过程:
(一)[猜想I]:主要成分为氯化铵;
[验证(操作)过程]:取少量滤液加入NaOH固体,并加热;
[实验现象]:闻到有轻微的氨味;
[判断猜想]: (填“猜想I成立”或“猜想I不成立”);
(二)[猜想II]:主要成分为氯化锌;
[验证(操作)过程]: ;
[实验现象]: ;
[判断猜想]:猜想Ⅱ成立;
由上述实验得出的结论是:滤液中的主次成分: 。
查看答案和解析>>
科目: 来源: 题型:
(1)对下列仪器:
A.容量瓶 B.蒸馏烧瓶 C.滴定管 D.量筒
E.烧杯 F.蒸发皿 G.分液漏斗
使用时必须检查是否漏水的有 (填序号)
(2)用固体NaOH配制250mL0.5mol·L-1 NaOH溶液, 下列操作使所配制的NaOH溶液
浓度偏高的有:______________(填写代号)。
A.称取固体NaOH时未用小烧杯
B.没有用水冲洗烧杯2~3次
C.定容时,俯视液面使与刻度相切
D.溶液配好摇匀后,发现液面低于刻度线,又加水至液面与刻度相切
E.将未冷却的溶液注入容量瓶后,马上定容
F.样品中混有Na2O杂质
(3)下图各种尾气吸收装置中,适合于吸收HCl气体,而且能防止倒吸的有_________。
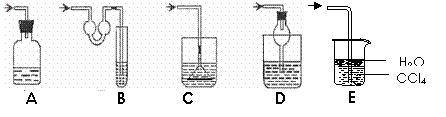
查看答案和解析>>
科目: 来源: 题型:
向某FeBr2溶液中,通入1.12L(标准状况下)的Cl2,测得溶液中c(Br-)=3c(Cl—)=0.3mol/L。反应过程中溶液的体积变化不计,则下列说法中正确的是 ( )
A.原溶液的浓度为0.1mol/L
B.反应后溶液中c(Fe3+)=0.1mol/L
C.反应后溶液中c(Fe3+)=c(Fe2+)
D.原溶液中c(Br-)=0.4mol/L
查看答案和解析>>
科目: 来源: 题型:
关于下列各装置图的叙述中,不正确的是 ( )
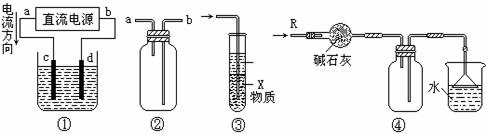
A.装置①中,d为阳极、c为阴极
B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体
C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
查看答案和解析>>
科目: 来源: 题型:
.已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是 ( )
A.上述实验证明氧化性:![]() >Cl2>Fe3+>I2
>Cl2>Fe3+>I2
B.上述实验中,共有两个氧化还原反应
C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝
D.实验②证明Fe2+既有氧化性又有还原性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com