
科目: 来源: 题型:
下列关于分散系的说法,正确是………………………………………………( )
A.稀硫酸不是分散系
B.一种分散系里只有分散质和分散剂两种物质
C.分散剂一定是液体
D.按分散质和分散剂的状态(气、液、固态),有9种组合方式
查看答案和解析>>
科目: 来源: 题型:
配制一定体积、一定物质的量浓度的溶液时,下列会使配得的溶液浓度偏小的是( )
A. 容量瓶中原有少量蒸馏水
B. 溶液从烧杯转移到容量瓶中后洗涤了烧杯
C.定容时观察液面俯视
D.定容时倒转容量瓶几次,发现凹液面最低点低于标线,再补几滴水到标线
查看答案和解析>>
科目: 来源: 题型:
下列离子反应方程式,书写正确的是( )
A. 向碳酸钠溶液中加盐酸 CO32- + 2H+ = H2O +CO2 ↑
B.向稀硫酸溶液中投入铁粉 2Fe +6H+ = 2Fe3+ +3H2 ↑
C. 向盐酸中投入碳酸钙 CO32- + 2H+ = H2O +CO2 ↑
D. 氢氧化钡溶液中加入硫酸 H+ + OH- =H2O
查看答案和解析>>
科目: 来源: 题型:
下列反应中,铁元素被氧化的是…………………………………………….( )
A.FeS +2HCl = FeCl2 + H2S↑ B. Fe +H2SO4 = FeSO4 +H2↑
C. FeO + 2HCl =FeCl2 +H2O D. Fe2O3 +3CO = 2Fe +3CO2
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是 ( )
A.1 mol H2O的质量为18g/mol
B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g
D.标准状况下,1 mol任何物质体积均为22.4L
查看答案和解析>>
科目: 来源: 题型:
下列电离方程式,书写正确的是( )
A. Al2(SO4)3 =2Al3+ + 3SO42- B.AlCl3 = Al3+ +Cl3-
D. Mg(NO3)2 = Mg+2 +2NO3- D.KMnO4 =K+ +Mn7+ +4O2-
查看答案和解析>>
科目: 来源: 题型:阅读理解
美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如下图:
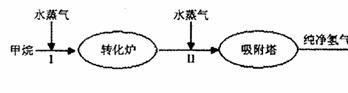
(1)此流程的第II步反应为:CO(g)+H2O(g)![]() H2(g)+CO2(g),该反应的化学平衡常数表达式为K= ;反应的平衡常数随温度的变化如表一,
H2(g)+CO2(g),该反应的化学平衡常数表达式为K= ;反应的平衡常数随温度的变化如表一,
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
从上表可以推断:此反应是_______________ (填“吸”、“放”)热反应。
在830℃下,若开始时向恒容密闭容器中充入CO与HzO均为1 mo1,则达到平衡后
CO的转化率为_____。
(2)此流程的第II步反应CO(g)+H2O(g)![]() H2(g)+CO2(g),在830℃,以表二的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有 (填实验编号);
H2(g)+CO2(g),在830℃,以表二的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有 (填实验编号);
| 实验编号 | N(CO) | N(H2O) | n(H2) | N(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 0.5 | 2 | 1 | 1 |
(3)在一个不传热的固定容积的容器中,判断此流程的第II步反应达到平衡的标志是
 ① 体系的压强不再发生变化 ②混合气体的密度不变
① 体系的压强不再发生变化 ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④ 各组分的物质的量浓度不再改变
⑤ 体系的温度不再发生变化 ⑥ v(CO2正)= v(H2O逆)
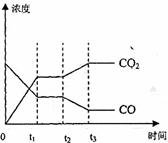
(4) 图表示该反应此流程的第II步反应在时刻
t![]() 达到平衡、在时刻t
达到平衡、在时刻t![]() 分别因改变某个条
分别因改变某个条
件而发生变化的情况:图中时刻t![]() 发生改
发生改
变的条件是_________。(写出两种)
(5)若400℃时,第Ⅱ步反应生成l mol氢气的热量数值
为 33.2(单位为kJ),第Ⅰ步反应的热化学方程式为:
CH4(g)+H2O(g)=3H2(g)+CO(g)△H=-103.3 kJ·mol-1。
则400℃时,甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
某实验小组同学对电化学原理进行了一系列探究活动。
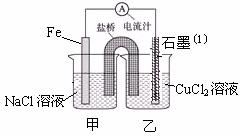 (1)下图为某实验小组依据氧化还原反应:(用离子方程式表示) 设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12g,导线中通过 mol电子。
(1)下图为某实验小组依据氧化还原反应:(用离子方程式表示) 设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12g,导线中通过 mol电子。
(2)其它条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为 ,
这是由于NH4Cl溶液显 性,(填酸性、碱性或中性)用离子方程式表示溶液显此性的原因 ,用吸管吸出铁片附近溶液少许至于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式 ,然后滴加几滴硫氰化钾溶液,溶液变红,继续滴加过量新制饱和氯水,颜色褪去,同学们对此做了多种假设,某同学的假设是:“溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为FeO42-,试写出该反应的离子方程式 。
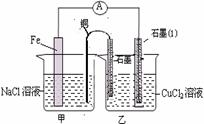 (3)如图其它条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示,
(3)如图其它条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示,
一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是 ,电极反应为 ;乙装置中石墨(1)为 极(填正、负、阴、阳),乙装置中与铜线相连石墨电极上发生的反应式为 ,产物常用
检验,反应的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com