
科目: 来源: 题型:
将0.1mol Cu与40ml 10mol/LHNO3充分反应,测得反应后的溶液里含有a molH+
由此可知
A.生成的气体一定是NO2,在标准状况下的体积4.48 L
B.生成的气体一定是NO,在标准状况下的体积约1.49L
C.被还原的硝酸的物质的量为(0.2-a)mol
D.反应后的溶液里含有0.2mol NO3-
查看答案和解析>>
科目: 来源: 题型:
分类是学习和研究化学的一种常用的科学方法。下列分类合理的是
①根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
②根据电解质在熔融状态下能否完全电离将电解质分为强电解质和弱电解质
③根据元素原子最外层电子数的多少将元素分为金属和非金属
④根据反应的热效应将化学反应分为放热反应和吸热反应
A.②③ B.②③④ C.①② D.①④
查看答案和解析>>
科目: 来源: 题型:
实验室中有一瓶氯化钾和氯化钙的固体混和物,通过下面的实验可制得纯净的氯化钾。根据实验步骤填写下列空白。
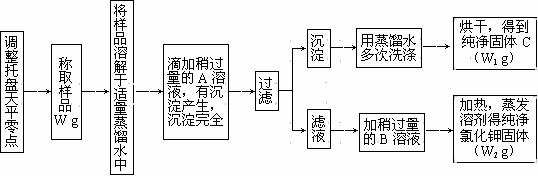 |
⑴ 加入的A是 ,检验A是否过量的方法是 。
⑵ 除烧杯、漏斗外,上述实验中的过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是 。
⑶ 滤液中加入的B物质是 。应该加入过量的B物质,理由是 。
⑷ 得到的固体C是 。
⑸ 为检验提纯的KCl的纯度,需配制500 mL4.00 mol·L-1KCl(纯KCl)溶液,所用的定量仪器除天平、量筒外还有 (填仪器名称),需要KCl固体 g。
⑹ 若要确定该混和物中氯化钾和氯化钙的质量比,需要用到上述实验数据中的 w g和 。
查看答案和解析>>
科目: 来源: 题型:
实验室有两瓶溶液,都已失去标签,已知其中一瓶是硫酸溶液,另一瓶是蔗糖溶液。同学们设计了下列方案对溶液进行鉴别:
A. 用pH试纸分别测定两溶液的pH,pH < 7的是硫酸溶液,pH = 7的是蔗糖溶液。
B. 取样,分别向两溶液中滴加盐酸酸化的氯化钡溶液,生成白色沉淀的是硫酸溶液,不产生沉淀的是蔗糖溶液。
C. 取样,分别向两溶液中加入一小片铜片,产生气体的是硫酸溶液,不产生气体的是蔗糖溶液。
D. 取样,分别进行导电性实验,能导电的是硫酸溶液,不能导电的是蔗糖溶液。
E. 分别取极少量溶液尝一尝,有甜味的是蔗糖溶液,有酸味的是硫酸溶液。
⑴ 上述实验方案及结论正确的是 (填序号)。
⑵ 请你设计另一个实验方案鉴别硫酸溶液和蔗糖溶液。 。
查看答案和解析>>
科目: 来源: 题型:
工业上对海水资源综合开发利用的部分工艺流程如下图所示。
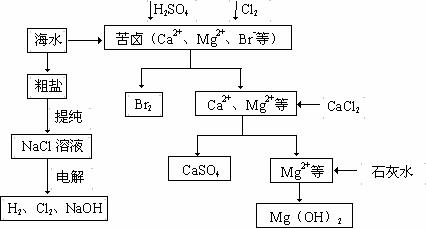 |
⑴ 粗盐中含有Ca2+、Mg2+、SO42-等杂质,粗制后可得饱和NaCl溶液,精制时通常在溶液中依次中加入过量的BaCl2溶液、过量的NaOH溶液和过量的Na2CO3溶液,过滤后向滤液中加入盐酸至溶液呈中性。请写出加入Na2CO3溶液后相关化学反应的离子方程式 。
⑵ 从海水中提取溴,主要反应为2Br- + Cl2 = Br2 + 2Cl-,下列说法错误的是 (填序号)。
A. 溴离子具有氧化性 B. 氯气是还原剂
C. 该反应属于复分解反应 D. 氯气的氧化性比溴单质强
⑶ 本工艺流程中先后制得Br2、CaSO4、Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4的顺序制备? (填“能”或“否”),原因是 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
我们生活中的许多现象及大量物质的应用都与氧化还原反应有关。请运用氧化还原反应的知识回答下列问题。
⑴ 氯气与水反应生成的次氯酸(HClO)具有杀菌作用,常用于自来水的消毒。在次氯酸(HClO)中,氯元素的化合价为 ,氯原子容易得到电子,从而使氯元素化合价降低,因此次氯酸具有 。次氯酸具有漂白作用就是基于它的这个性质。
⑵ 氮化铝(AlN)具有耐高温、抗冲击,导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
Al2O3 + N2 + 3C = 2AlN + 3CO
① 在化学方程式上标出该反应中电子转移的方向和数目。
② 在该反应中,还原剂是(写化学式) ,氧化产物是(写化学式) 。
⑶ 一个体重 50 kg的健康人,体内约有2 g铁,这2 g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体的吸收。
① 在人体中进行Fe2+ ![]() Fe3+的转化时,a中的Fe2+作 剂,b中的Fe3+作 剂。
Fe3+的转化时,a中的Fe2+作 剂,b中的Fe3+作 剂。
② “服用维生素C,可使食物中的Fe3+还原成Fe2+”这句话指出,维生素C在这一反应中作 剂,具有 性。
③ 市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化为亚铁盐,此反应的离子方程式为 。
查看答案和解析>>
科目: 来源: 题型:
甲、乙、丙、丁分别是盐酸、碳酸钠、氯化钙、硝酸银4种溶液中的一种。将它们两两混合后,观察到的现象是:① 甲与乙或丙混合都产生沉淀;② 丙与乙或丁混合也产生沉淀;③ 丁与乙混合产生无色气体。回答下列问题:
⑴ 写出丁与乙反应的离子方程式: 。
⑵ 这四种溶液分别是甲: 、乙: 、丙: 、丁: (写化学式)。
查看答案和解析>>
科目: 来源: 题型:
下列反应完成后没有沉淀的是
A. BaCl2溶液与Na2CO3溶液加足量稀HCl
B. Ba(OH)2溶液与KNO3溶液加足量稀H2SO4
C. AgNO3溶液与Na2CO3溶液加足量稀HCl
D. Ca(OH)2溶液与FeCl3溶液加足量稀HNO3
查看答案和解析>>
科目: 来源: 题型:
下列反应的离子方程式正确的是
A. 将打磨过的铝片放入氯化铜溶液中:Al + Cu2+ = Al3+ + Cu
B. CuSO4溶液与Ba(OH)2溶液混合:Cu2+ + SO42- + Ba2+ + 2OH- BaSO4↓+ Cu(OH)2↓
C. 往澄清石灰水中通入过量二氧化碳: Ca2+ + 2OH- + CO2 CaCO3↓+ H2O
D. 氢氧化铁与稀硫酸反应:Fe(OH)3 + 3H+ = Fe3+ +3H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com