
科目: 来源: 题型:阅读理解
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示可逆反应进行得越完全,K值大小与温度的关系是:温度升高,K值_______________(填“一定增大”“一定减小”或“可能增大也可能减小”)。
(2)在一体积为10L的容器中,通入一定量的CO和H2O,在800℃时发生如下反应:
CO(g)+H2O (g) ![]() CO2(g)+H2 (g) △H<0
CO2(g)+H2 (g) △H<0
CO和H2O物质的量浓度变化如下图(a)所示,则:
① 0-4min间平均反应速率v(CO)=________ mol•L-1•min-1
②在800℃时该反应的化学平衡常数K=___________________________(要求写出表达式及数值);CO的转化率=______________。
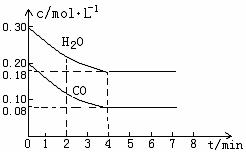
图(a)
③在800℃时,若反应开始时此容器中CO和H2O的浓度分别为0.20 mol/L和0.80 mol/L,则达到平衡时CO转化为CO2的转化率是:______________________。
(3)25℃时,Ksp[Mg(OH)2]=5.61×10-12,Ksp[MgF2]=7.42×10-11。下列说法正确的是_______
A.25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比, c(Mg2+)后者大
B.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)减小
C.25℃时,Mg(OH)2固体在20mL0.01mol·L-1氨水中的Ksp和在20mL0.01 mol·L-1
NH4Cl溶液中的Ksp相等
D.25℃时,在Mg(OH)2悬浊液中加入NaF溶液后,Mg(OH)2可能转化为MgF2
E.25℃ 时,某饱和Mg(OH)2溶液中c(Mg2+)=0.0561mol·L-1,则溶液的pH=9
(4)根据化学反应速率与化学平衡理论,联系化工生产实际,你认为下列说法不正确的是 。
A.化学反应速率理论可指导怎样在一定时间内快出产品
B.有效碰撞理论可指导怎样提高原料的转化率
C.勒夏特列原理可指导怎样使用有限原料多出产品
D.催化剂的使用是提高产品率的有效方法
E.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益
查看答案和解析>>
科目: 来源: 题型:
(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是________。
A. KMnO4 B. H2O2 C. 氯水 D. HNO3
然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________。
A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为________,Fe3+完全沉淀时溶液的pH为________,通过计算确定上述方案________(填“可行”或“不可行”)。 ( 提示: lg5 =0.7)
查看答案和解析>>
科目: 来源: 题型:
I.有关中和滴定的操作有: ①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液 ③检查滴定管是否漏水 ④滴定 ⑤洗涤
正确的操作顺序是 (填字母)
A. ⑤①②③④ B. ③⑤①②④ C. ⑤②③①④ D. ②①③⑤④
Ⅱ.氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001mol·L-1KMnO4酸性溶液和未知浓度的无色NaHSO3溶液。反应的离子方程式是:2MnO4-+5HSO3-+H+ = 2Mn2++5SO42-+3H2O
填空回答下列问题:
(1)不用 (填“酸式”或“碱式”)滴定管盛放高锰酸钾溶液。
(2)选何种指示剂 。(填序号)
①甲基橙 ②酚酞 ③ 石蕊 ④不用指示剂
(3)滴定前平视KMnO4液面,刻度为a mL,滴定后俯视液面刻度为b mL,则
(b-a)mL比实际消耗KMnO4溶液体积 (填“多”或“少”)。根据(b-a)mL计算得到的待测液浓度,比实际浓度 (填“大”或“小”)。
(4)无论是KMnO4溶液往NaHSO3溶液中滴,还是NaHSO3溶液往KMnO4溶液中滴,在其他操作正确规范的前提下,下列操作一定会使测定结果偏高的是 。(填序号)
①取用NaHSO3溶液的滴定管未用待测NaHSO3溶液润洗
②取用KMnO4酸性溶液的滴定管未用标准KMnO4酸性溶液润洗
③滴定过程中不慎有液体溅出
④滴定前仰视读数,滴定后平视读数
查看答案和解析>>
科目: 来源: 题型:
25℃时,①氢氟酸、②醋酸、③次氯酸的电离常数分别是3.5×10-4、1.8×10-5、3.0×10-8。请推测:它们的酸性由强到弱的顺序为______________________(填序号,下同),相同浓度的溶液中,氢离子浓度最大的是__________,电离程度最小的是_______;相同浓度的④氟化钠溶液、⑤醋酸钠溶液、⑥次氯酸钠溶液pH的从大到小顺序:_____________________________。
查看答案和解析>>
科目: 来源: 题型:
以铁为阳极,铜为阴极,对足量的NaOH溶液进行电解。一段时间后得到4mol Fe(OH)3沉淀,此间共消耗的水的物质的量为
A.8mol B.10mol C.11mol D.12mol
查看答案和解析>>
科目: 来源: 题型:
常温下,某强酸溶液的PH=a,强碱溶液的PH=b,已知a+b=12,酸碱溶液混合后PH=7,则酸溶液的体积V(酸)和碱溶液体积V(碱)的正确关系是
A.V(酸)=102V(碱) B.V(碱)=102V(酸)
C.V(酸)=2V(碱) D.V(碱)=2V(酸)
查看答案和解析>>
科目: 来源: 题型:
在密闭容器中,对于可逆反应A+3B 2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
A.若正反应方向的△H<0,则T1>T2
B.A一定为气体
C.B一定为气体
D.压强增大时,混合气体的平均相对分子质量一定减小
查看答案和解析>>
科目: 来源: 题型:
有等体积、等pH的Ba(OH)2、NaOH和NH3·H2O三种碱溶液,滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是
A.V3>V2>V1 B.V1>V2>V3 C.V3>V2=V1 D.V1=V2>V3
|
查看答案和解析>>
科目: 来源: 题型:
将pH= l的盐酸平均分成 2份,l份加适量水,另1份加入与该盐酸物质的量浓度相同的适量NaOH溶液后,pH都升高了1,则加入的水与NaOH溶液的体积比为
A. 9 B.10 C.11 D.12
查看答案和解析>>
科目: 来源: 题型:
20℃时H2S饱溶液1L,其浓度为0.1mol·L-1,其电离方程式为H2S![]() H++HS-,HS-
H++HS-,HS-![]() H++S2-,若要使该溶液[H+]及[S2-]都减小,可采取的措施是
H++S2-,若要使该溶液[H+]及[S2-]都减小,可采取的措施是
A.加入适量的水 B.加入适量的NaOH固体
C.通入适量的Cl2 D.加入适量的CuSO4固体高考资源网
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com