
科目: 来源: 题型:
实验探究是体验知识的产生和形成过程的基本途径。下面是某同学完成的探究实验报告的一部分:
实验名称:卤素单质的氧化性强弱比较
实验药品:KBr溶液、KI溶液、氯水、溴水、碘水、四氯化碳、淀粉碘化钾试纸
实验设计如下,请回答:
(1)完成该实验需用到的实验仪器是 、 。
(2) ②中反应的化学方程式为
③中反应的离子方程式为
(3)CCl4在实验中所起的作用是 。
(4)该同学的实验设计不足之处是 ,
改进的办法是 。
查看答案和解析>>
科目: 来源: 题型:
已知X、Y、Z、W四种短周期元素的位置如右图所示,X形成的单质约占空气体积的1/5,四种元素原子核外共有56个电子,请回答下列问题:
| X | ||
| Y | Z | W |
(1)Y的元素符号是 ;
| 实验步骤 | 实验结论 |
| ①氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 | 氧化性 从强到弱 的顺序: 氯、溴、碘 |
| ②NaBr溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 | |
| ③KI溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 |
(2)X与Na形成淡黄色固体化合物的化学式是 ,该化合物与二氧化碳反应的化学方程式是_______________________________________________________________。
(3)ZX2能使品红溶液褪色,ZX2的化学式是 说明ZX2具有_________性。
(4)W2与氢氧化钠溶液反应的离子方程式是_____________________________。
查看答案和解析>>
科目: 来源: 题型:
元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑩九种元素在周期表中的位置。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ⑩ | ||||||
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ③ | ④ | ⑧ | ||||
| 4 | ⑤ | ⑨ |
请回答:(以下用相应的元素符号回答问题)
(1) 在表里填写①—⑩元素符号,写出元素符号① 、③ 、⑧
(2)其中化学性质最不活泼的是 (填元素符号)。
(3) 在②、③、④三种元素的氧化物对应的水化物中,碱性最强的是
(填化学式)。
(4) 元素①、②、⑤按原子半径由大到小的顺序依次为 (填元素符号),原因 。
(5)元素⑥的氢化物的化学式是 ,该氢化物溶于水,所得溶液的
pH (填“<”、“>”或“=”)7。该氢化物与水发生反应的化学方程式为 。
(6) 元素②与元素⑧形成的化合物的化学式是 ;电子式是 ,高温下灼烧该化合物火焰呈 色。
(7) (填化学式)的单质既可以和盐酸又可以和氢氧化钠溶液反应,其单质与氢氧化钠溶液反应的化学方程式是
查看答案和解析>>
科目: 来源: 题型:
在右图所示的原电池中,下列说法正确的是
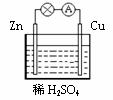 A.Zn为负极,Cu为正极
A.Zn为负极,Cu为正极
B.正极反应为 Zn - 2e- == ![]()
C.负极反应为Cu - 2e- == ![]()
D.该装置能将电能转化为化学能
查看答案和解析>>
科目: 来源: 题型:
某主族元素R的最高正价与最低负化合价的代数和为4,由此可以判断( )
A.R一定是第四周期元素
B.R一定是ⅣA族元素
C.R的气态氢化物比同族其他元素气态氢化物稳定
D.R气态氢化物化学式为H2R
查看答案和解析>>
科目: 来源: 题型:
铊是超导材料的组成元素之一,铊在周期表中位于第六周期,与铝是同族元素,元素符号是Tl,以下对铊的性质的推断正确的是( )
A.Al的金属性强于Tl B.能生成+3价的共价化合物
C.铊是易导电的银白色金属 D.Tl2O3与Al2O3都具有两性
查看答案和解析>>
科目: 来源: 题型:
同周期的X、Y、Z三种元素,已知其最高价氧化物对应的水化物的酸性强弱顺序是:HXO4>H2YO4>H3ZO4,则下列各判断中正确的是( )
A.原子半径:X>Y>Z B.单质的非金属性:X>Y>Z
C.气态氢化物稳定性:X<Y<Z D.原子序数:X<Y<Z
查看答案和解析>>
科目: 来源: 题型:
下列各组中化合物的性质比较,不正确的是( )
A.酸性:HClO4>H2SO4>H3PO4 B.碱性:NaOH>Mg(OH)2>Al(OH)3
C.酸性:HI>H Br>H Cl D.非金属性: O>F>S
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com