
科目: 来源: 题型:
有可逆反应A+B![]() 2C在不同温度下经过一定时间,混合物中C的百分含量与温度关系如下图所示,那么:
2C在不同温度下经过一定时间,混合物中C的百分含量与温度关系如下图所示,那么:
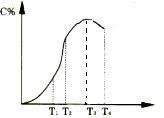 (1)反应在___________________温度下达到化学平衡;
(1)反应在___________________温度下达到化学平衡;
(2)此正反应为______________________热反应;
(3)由T1向T2变化时,V正____________V逆(填>、<、=);
(4)由T3向T4变化时,V正_____________V逆(填>、<、=).
查看答案和解析>>
科目: 来源: 题型:
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示__________, K值大小与温度的关系是:温度升高,K值_________________。(填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
 CO(g) +H2O(g)
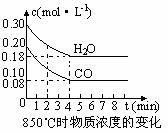
CO(g) +H2O(g) ![]() CO2(g) +H2 (g) △H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=_________mol·L-1·min-1。
CO2(g) +H2 (g) △H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=_________mol·L-1·min-1。
| 时间(min) | CO | H2 | CO | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
T℃时物质浓度(mol·L-1)的变化:
(3)T℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min~4min之间反应处于_________状态; c 1数值_________0.08 mol·L-1 (填大于、小于或等于)。
②反应在4min~5min间,平衡向逆方向移动,可能的原因是_________ (单选),表中5min~6min之间数值发生变化,可能的原因是_________ (单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
查看答案和解析>>
科目: 来源: 题型:
已知可逆反应CO(g)+H2O(g) ![]() CO2(g) + H2(g),
CO2(g) + H2(g),
(1)写出该反应的化学平衡常数表达式:K= 。
(2)830K时,若起始时:C(CO)=2mol/L,C(H2O)=3mol/L,平衡时CO的转化率为60%,水蒸气的转化率为 ;K值为 。
(3)830K时,若只将起始时C(H2O)改为6mol/L,则水蒸气的转化率为 。
(4)若830K时,起始浓度 C(CO) = a mol/L, C(H2O) = b mol/L,H2的平衡浓度为
C(H2) = c mol/L,则:
①a、b、c之间的关系式是 ;②当a=b时,a= c。
查看答案和解析>>
科目: 来源: 题型:
I.恒温、恒压下,在一个可变容积的容器中发生如下发应:A(g)+B(g)![]() C(g)
C(g)
(1)若开始时放入1molA和1molB,到达平衡后,生成a molC,这时A的物质的量为 mol。
(2)若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为 mol。
(3)若开始时放入x molA,2molB和1molC,到达平衡后,A和C的物质的量分别是ymol和3a mol,则x= mol,y= mol。平衡时,B的物质的量 (选填一个编号)(甲)大于2 mol (乙)等于2 mol(丙)小于2 mol (丁)可能大于、于或小于2mol作出此判断的理由是 。
(4)若在(3)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是 。
II.若维持温度不变,在一个与(1)反应前起始体积相同、且容积固定的容器中发生上述反应。
(5)开始时放入1molA和1molB到达平衡后生成b molC。将b与(1)小题中的a进行比较 (选填一个编号)。
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和b的大小
作出此判断的理由是 。
查看答案和解析>>
科目: 来源: 题型:
有等体积、等pH的Ba(OH)2、NaOH和NH3·H2O三种碱溶液,滴加等物质的量浓度的盐酸将它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是
A.V3>V2>V1 B.V1=V2=V3 C.V3>V2=V1 D.V1=V2>V3
查看答案和解析>>
科目: 来源: 题型:
pH值相同的盐酸溶液和醋酸溶液分别和锌反应,若最后锌都已完全溶解,放出的氢气一样多,则下列判断正确的是
A.整个反应阶段平均速率:醋酸>盐酸 B.反应所需时间:醋酸>盐酸
C.参加反应的锌的质量:盐酸<醋酸 D.开始反应速率:盐酸>醋酸
查看答案和解析>>
科目: 来源: 题型:
将等物质的量的X、Y气体充入某密闭容器中,在一定条件下,发生如下反应并达到平衡:X(g)+3Y(g)![]() 2Z(g) △H<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是
2Z(g) △H<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是
| 改变条件 | 新平衡与原平衡比较 | |
| A | 升高温度 | X的转化率变小 |
| B | 增大压强 | X的浓度变小 |
| C | 充入一定量Y | Y的转化率增大 |
| D | 使用适当催化剂 | X的体积分数变小 |
查看答案和解析>>
科目: 来源: 题型:
实验室用足量镁粉与一定量的某浓度的盐酸反应来制得氢气。由于反应速率太快,不易操作。为减慢反应速率,同时又不影响生成H2的总量,可向盐酸中加入的物质是
A、CH3COONa固体 B、NaOH溶液 C、(NH4)2 SO4粉末 D、K2 SO4固体
查看答案和解析>>
科目: 来源: 题型:
室温下,下列溶液等体积混和,所得溶液pH的一定大于7的是
A、0.1mol.l-1盐酸溶液和0.1mol.l-1氢氧化钠溶液
B、0.1mol.l-1盐酸溶液和0.1mol.l-1氢氧化钡溶液
C 、pH =4醋酸溶液和pH =10氢氧化钠溶液
D、 pH =4盐酸溶液和pH =10氢氧化钡溶液
查看答案和解析>>
科目: 来源: 题型:
恒温时, 容积不变的密闭容器中充入1molNO2,建立如下平衡:2NO2 (g) ![]() N2O4(g),测得NO2的转化率为a﹪其他条件不变,再充入1molNO2,新平衡建立时测得NO2的转化率为b﹪,则a与b的关系为
N2O4(g),测得NO2的转化率为a﹪其他条件不变,再充入1molNO2,新平衡建立时测得NO2的转化率为b﹪,则a与b的关系为
A. a>b B. a<b C . a=b D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com