
科目: 来源: 题型:
常温下,向0.1 mol·L-1的CH3COONa溶液中逐滴滴加等浓度的HCl溶液,则下列关系正确的是
A.c(H+)·c(OH-)=1×10-14
B.c(Na+)+c(H+)=c(OH-)+c(CH3COO-)
C.c(Na+)=c(CH3COOH)+c(CH3COO-)
D.c(Na+)=c(Cl-)>c(H+)>c(CH3COO-)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
已知X、Y、Z、W是四种短周期非金属元素,在周期表中的相对位置如下图所示,下列说法不正确的是( )

A.Z元素的最高化合价可能比Y元素的高
B.X、Y、Z、W的氢化物中,X的氢化物沸点可能最低
C.Z的单质为原子晶体时,W的单质可能为分子晶体
D.X的最高价氧化物对应水化物与其氢化物不可能相互反应
查看答案和解析>>
科目: 来源: 题型:
14g铜、银合金与足量的某浓度的硝酸反应,将放出气体与1.12L(标准 壮况下)氧气混合,通入水中恰好全部被吸收,则合金中铜的质量是
A.9.6g B.6.4g C.3.2g D.1.6g
查看答案和解析>>
科目: 来源: 题型:
在盛有少量无水乙醇的试管中,加入一小块新切的、擦干表面煤油的金属钠,迅速用配有导管的单孔塞塞住试管口,用一小试管收集并验纯气体后,点燃,并把干燥的小烧杯罩在火焰上,片刻,迅速倒转烧杯,向烧杯中加入少量澄清石灰水。

观察现象,完成下表。
| 乙醇与钠反应的现象 | 气体燃烧的现象 | 检验产物 |
|
| 气体燃烧时火焰呈 , 小烧杯内壁 , 澄清石灰水 。 | 反应中只生成了
|
写出乙醇与钠反应的化学方程式
查看答案和解析>>
科目: 来源: 题型:
对达到平衡状态的可逆反应X+Y![]() Z+W,在其他条件不变的情况下,增大压强,反应速率变化图象如图所示,则关于X、Y、Z、W四种物质的聚集状态说法正确的是( )
Z+W,在其他条件不变的情况下,增大压强,反应速率变化图象如图所示,则关于X、Y、Z、W四种物质的聚集状态说法正确的是( )
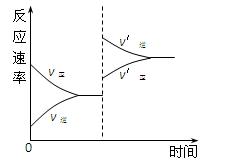
A.X、Y均为气体,Z、W中有一种为气体
B.Z、W中有一种是气体,X、Y皆非气体
C.X、Y、Z、W皆非气体
D.Z、W均为气体,X、Y中有一种是气体
查看答案和解析>>
科目: 来源: 题型:
下列关于实验问题处理方法或操作不正确的是
A.实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
B.在实验室,不能品尝药品
C.熄灭实验桌上燃着的酒精,简便合理的方法就是用湿抹布盖灭
D.配制稀硫酸时,先在烧杯中加一定体积的水,再边搅拌边沿杯壁加入浓硫酸
查看答案和解析>>
科目: 来源: 题型:
鲨鱼是世界上惟一不患癌症的动物,科学研究表明,鲨鱼体内含有一种角鲨烯,具有抗癌性。实验测得角鲨烯分子是链状结构,分子中含有30个碳原子且碳、氢元素质量比为7.2∶1,下列说法中不正确的是
A.角鲨烯分子式为C30H50
B.角鲨烯与分子式为C29H48的物质可能属于同系物
C.角鲨烯完全加氢后为C30H62
D.1 mol角鲨烯最多可与5mol溴单质加成
查看答案和解析>>
科目: 来源: 题型:
类推思维是化学解题中常用的一种思维方法,下列有关反应方程式的类推正确的是
| 已知 | 类推 | |
| A | 将Fe加入CuSO4溶液中 Fe+Cu2+=Cu+Fe2+ | 将Na加入到CuSO4溶液中 2Na+Cu2+=Cu+2Na+ |
| B | 稀硫酸与Ba(OH)2溶液反应至中性 2H++SO | NaHSO4溶液与Ba(OH)2溶液反应至中性 2H++ SO |
| C | 铁和氯气反应 2Fe+3Cl2 | 铁和碘单质反应 2Fe +3I2 |
| D | 向Ca(ClO)2溶液中通入少量CO2 Ca2++2ClO—+CO2+H2O=CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2 Ca2++2ClO—+SO2+H2O=CaSO3↓+2HClO |
查看答案和解析>>
科目: 来源: 题型:阅读理解
氨是一种重要的化工原料,氨的合成与应用是当今重要研究内容之一。不同温度、压强下,合成氨平衡体系中NH3的物质的量分数见下表(N2和H2起始物质的量之比为1∶3)。
|
衡含量(%) 温度(℃) | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
回答下列有关问题:
(1)利用表中数据推断得出合成氨的反应是__________反应(填“放热”、“吸热”或“无热量变化”)。
(2)根据表中数据,在200℃和100MPa时,平衡体系中NH3的物质的量分数最高,而实际工业生产不选用该条件的主要原因是___________________________________。
(3)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减小”或“可能增大也可能减小”):
| 反应速率 | 平衡常数K | 氨的体积分数 | |
| 变化情况 |
(4)将1molH2和1molN2通入一体积不变的密闭容器中,在一定温度和催化剂作用下,反应达到平衡,测得NH3的物质的量为0.3mol,此时若移走0.5molH2和0.5molN2,则反应达到新的平衡时,NH3的物质的量为_____________(选填答案编号)。
A.0.3mol B.0.15mol C.小于0.15mol D.大于0.15mol,小于0.3mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com