
科目: 来源: 题型:
下列叙述正确的是
A.汽油、柴油和植物油都是碳氢化合物
B.乙醇可以被氧化为乙酸,二者都能发生酯化反应
C.甲烷、乙烯和苯在工业上都可通过石油分馏得到
D.含5个碳原子的有机物,每个分子中最多可形成4个C—C单键
查看答案和解析>>
科目: 来源: 题型:
25 ℃时,下列各溶液中,粒子的物质的量浓度关系不正确的是( )
A、0.1 mol/L NH4Cl溶液中加入NH 3·H2O 至呈中性时:c(NH4+ )=c(Cl-)
B、0.1 mol/L Na2CO3溶液中:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
C、向硝酸钠溶液中滴加稀盐酸得到的pH=3的混合溶液中:c(Na+)=c(NO3)-
D、CH3COONa溶液中加入适量CH3COOH,所得酸性混合溶液:
c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
有8种物质:①乙烷;②乙烯;③乙炔;④苯;⑤甲苯;⑥溴乙烷;⑦聚丙烯;⑧环己烯。其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是
A.①②③⑤ B.④⑥⑦⑧ C.①④⑥⑦ D.②③⑤⑧
查看答案和解析>>
科目: 来源: 题型:
硫酸铵在强热条件下分解,生成氨、二氧化硫、氮气和水.反应中生成的氧化产物和还原产物的物质的量之比是(已知反应方程式为:3(NH4)2SO4===4NH3+3SO2+N2+H2O)
A.1:3 B.2:3 C.1:1 D.4:3
查看答案和解析>>
科目: 来源: 题型:
下列各组溶液,只要用试管和胶头滴管,不用任何试剂就可以鉴别的是
A. KOH和Al2(SO4)3 B. 稀H2SO4和NaHCO3
C. CaCl2和Na2CO3 D. Ba(OH)2和NaHSO4
查看答案和解析>>
科目: 来源: 题型:
25℃时,在某物质的溶液中,由水电离出的H+浓度为1??10-amol/L,下列说法正确的是
A、a <7时,水的电离受到抑制
B、a <7时,溶液的PH可能为a
C、a >7时,此溶液可能是NH4Cl溶液
D、a >7时,此溶液的PH值一定为14-a
查看答案和解析>>
科目: 来源: 题型:
硫酸工厂排放的尾气中,含少量的二氧化硫。为防止污染大气,在排放前必需进行尾气处理并设法进行综合利用。
⑴硫酸工厂排放尾气中的SO2通常用足量石灰水吸收,然后再用稀硫酸处理。
①写出上述过程的化学反应方程式: ,
②请说出这种尾气处理方法的优点(说出两点即可)
③若某硫酸厂每天排放的1万米3。(标准状况)尾气中含0.2%(体积百分数)的SO2,通过上述方法处理,理论上需生石灰 kg。
⑵近闻美国和日本正在研究用Na2SO3吸收法作为治理SO2污染的一种新方法,该方法:第一步是用Na2SO3水溶液吸收SO??2,第二步是加热吸收溶液,可得到含高浓度SO2的水蒸气副产品。
这种尾气处理方法与(1)相比的优点是 。
⑶某研究小组用NaOH溶液吸收尾气中的二氧化硫,将所得的Na2SO3溶液进行电解循环再生,这种新工艺叫再生循环脱硫法;其中阴阳膜组合循环再生机理如图,a、b离子交换膜将电解槽分为三个。区域,电极材料为石墨。
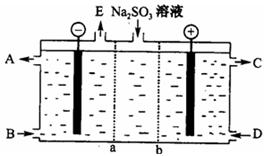
①图中a表示 离子交换膜(填“阴”或“阳”)。A—E分别代表生产中的原料或产品,其中C为硫酸,则A表示 ,E表示 。
②阳极的电极反应式为 。
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏加德罗常数,下列说法正确的是
A.标准状况下,5.6 L四氯化碳含有的分子数为0.25NA
B.1 mol C10H22分子中共价键总数为30NA
C.58.5g氯化钠可以构成NA个氯化钠晶胞
D.标准状况下,22.4 L任意比的氢气和氯气的混合气体中含有的分子总数均为NA
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.常温下0.4 mol/L HB溶液和0.2 mol/L NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c(Na+)>c(B-)>c(H+)>c(OH-)
B.常温时,pH =2的CH3COOH溶液和HC1溶液、pH=12的氨水和NaOH溶液,四种溶液中由水电离的c(H+)相等
C.常温下0.1 moil/L的下列溶液①NH4Al(SO4)2②NH4Cl③NH3·H2O④CH3COONH4中,c(NH4+)由大到小的顺序是:②>①>④>③
D.0.lmol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com