
科目: 来源: 题型:
下列离子方程式中正确的是
A.向KAl(SO4)2溶液中滴人过量Ba(OH)2溶液
2Ba2++ 4OH-+Al3++2SO42-=2BaSO4↓+AlO2- +2H2O
B.澄清石灰水与少量苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O
C.醋酸滴在石灰石上:CaCO3+2H+=Ca2++H2O+CO2↑
D.足量金属铝放入NaOH溶液:2Al+2OH- =2AlO- +3H2↑
查看答案和解析>>
科目: 来源: 题型:
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的元素。
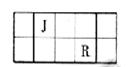
(1)元素T在周期表中位于第_________族。
(2)J和氢组成的化合物A每个分子由4个原子组成,其结构简式为________________,已知充分燃烧a gA物质时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则A物质燃烧热的热化学方程式是_______________________________。
(3)M和R形成的一种化合物能使酸性高锰酸钾溶液褪色,该反应的离子方程式为___________________________________________________。
(4)在微电子工业中,L的最简单气态氢化物的水溶液可作刻蚀剂H2O2 的清除剂,所发生反应的产物不污染环境,其化学方程式为:
___ __ _。
(5)写出三种仅由上述五种元素中的一种或两种元素形成的漂白剂的化学式:______________________。
(6)其中L、M、R形成的氢化物沸点由高到低的顺序是______________________(用化学式表示)
查看答案和解析>>
科目: 来源: 题型:
下列实验中说法正确的是
A.蒸发操作中,应使混合物中的水未完全蒸干时,就停止加热
B.将饱和FeCl3溶液滴入煮沸的NaOH溶液中,从而制得Fe(OH)3胶体
C.过滤操作不能用来分离胶体和溶液
D.开始蒸馏时,应该先加热蒸馏烧瓶,再开冷凝水;蒸馏完毕,应该先关冷凝水再撤酒精灯
查看答案和解析>>
科目: 来源: 题型:
配制500mL 1.0mol·L—1的NaOH溶液时,下列哪些操作会使实验结果偏高_____________;偏低__________;无影响______________。
A. 称量时,直接把氢氧化钠放在纸上称量,且称量时间过长
B. 称量时,固体放在右盘,砝码放在左盘
C. 称量时所用砝码生锈
D. 原容量瓶用蒸馏水洗净后未干燥
E . 移液后,未洗涤烧杯和玻璃棒
F. 定容时,俯视刻度线
G. 颠倒摇匀溶液后,发现液面低于刻度线,再补加水到刻度线
H. 溶液尚未冷却到室温就注入容量瓶进行定容
查看答案和解析>>
科目: 来源: 题型:
已知2A(g)+B(g)![]() 2C(g),向容积为1L的密闭容器中加入0.050 mol A和0.025mol B,在500℃时充分反应,达平衡后测得c(C)=0.040 mol·L-1,放出热量Q1kJ。
2C(g),向容积为1L的密闭容器中加入0.050 mol A和0.025mol B,在500℃时充分反应,达平衡后测得c(C)=0.040 mol·L-1,放出热量Q1kJ。
(1)能说明上述反应已经达到化学平衡状态的是 (填写序号);
a.v(C)=2v(B) b.容器内压强保持不变
c.v逆(A)=2v正(B) d.容器内气体的密度保持不变
(2)若在相同的容器中只加入0.050 mol C,500℃时充分反应达平衡后,吸收热量Q2kJ,则Q1与Q2之间的关系式可表示为 (用含Q1、Q2的代数式表示);
(3)500℃时,上述反应的化学平衡常数K= ;
(4)已知:K(300℃)>K(350℃),该反应是 (填“放”或“吸”)热反应;若反应温度升高,A的转化率 (填“增大”、“减小”或“不变”);
(5)某温度下,A的平衡转化率(a)与体系总压强(P)的关系如图所示,平衡状态由a变到b时,化学平衡常数K(A) K(B)(填“>”、“<”或“=”)。

查看答案和解析>>
科目: 来源: 题型:
今有①盐酸 ②硫酸 ③醋酸三种酸:
(1)在同体积,同PH的三种酸中,分别加入足量的锌粉,在相同条件下产生H2的体积由大到小的顺序是____________
(2)在同体积、同浓度的三种酸中,分别加入足量的锌粉,在相同条件下产生H2的体积由大到小的顺序是____________
(3)物质的量浓度为0.1 mol·L—1的三种酸溶液的PH由大到小的顺序是____________ _;如果取等体积的0.1 mol·L—1的三种酸溶液,用0.1 mol·L—1的NaOH溶液中和,当恰好完全反应时,消耗溶液的体积由大到小的顺序是____________ ___(以上均用酸的序号填写)。
查看答案和解析>>
科目: 来源: 题型:
已知:(1)Zn(s)+![]() O2(g)=== ZnO(s),ΔH1= -348.3 kJ·mol-1,
O2(g)=== ZnO(s),ΔH1= -348.3 kJ·mol-1,
(2)2Ag(s)+ ![]() O2(g)=== Ag2O(s),ΔH2=-31.0 kJ·mol-1,
O2(g)=== Ag2O(s),ΔH2=-31.0 kJ·mol-1,
则Zn(s)+ Ag2O(s) === ZnO(s)+ 2Ag(s)的ΔH等于( )
A.-379.3 kJ·mol-1 B.-317.3 kJ·mol-1
C.-332.8 kJ·mol-1 D.317.3 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
已知室温时,0.1 mol/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是 ( )
A.该溶液的pH=4
B.降低温度,溶液的pH减小
C.此酸的电离平衡常数约为1×10-7
D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
查看答案和解析>>
科目: 来源: 题型:
某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,以探索工业废料的再利用。其实验方案如下:
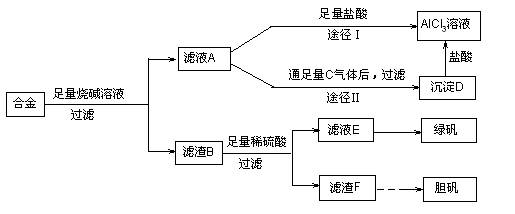
试回答下列问题:
(1)过滤用的器材已有:滤纸、铁架台、铁圈和烧杯,还要补充的玻璃仪器是 。(2)由滤液A制得AlCl3溶液有途径Ⅰ和Ⅱ两条,你认为合理的是 ,理由是 。
(3)从滤液E中得到绿矾晶体的实验操作是 。
(4)写出用滤渣F制备胆矾晶体的有关化学方程式 。
(5)有同学提出可将方案中最初溶解合金的烧碱改用盐酸,重新设计方案,也能制得三种物质,你认为后者的方案是否更合理 ,理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com