
科目: 来源: 题型:
已知C、D、E、F四种无机物均由短周期元素组成,且它们之间的转化关系如下:![]() 下列说法正确的是
下列说法正确的是
A. C为单质 B. E为氧化物
C. F为酸 D. C、D、E、F相对分子质量之差为16或16的倍数
查看答案和解析>>
科目: 来源: 题型:
图中a、b、c、d、e、f表示元素周期表中部分短周期元素,下列叙述正确的是
A.a、b、c的简单离子中,的离子半径最大
B.c、d、f最高价氧化物对应的水化物两两之间均可发生反应
C.e的氢化物比f的氢化物的稳定性高
D.a、e可形成一种新型无机非金属材料——高温结构陶瓷
查看答案和解析>>
科目: 来源: 题型:
在一容积为2 L的密闭容器中加入2 molA和3 molB,保持温度为30℃,在催化剂存在的条件下进行下列反应: ![]() ,达到平衡后生成1.2 mol C,此时,平衡混合气中C的体积分数为ω;若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为2.1 mol。
,达到平衡后生成1.2 mol C,此时,平衡混合气中C的体积分数为ω;若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为2.1 mol。
请回答下列问题,
(1)该反应的平衡常数K随温度升高而 (填“增大”、“减少”或“不变”),该反应的焓变△H 0(填“>”、“<”或“=”)。
(2)30℃时,平衡混合气中C的体积分数ω= ,A物质的转化率与B物质的转化率之比为 。
(3)30℃时,若在同一容器中加入3 molA、4 molB和 molC,则平衡混合气中C的体积分数仍为ω,此时平衡时体系中A的物质的量浓度为 mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置:
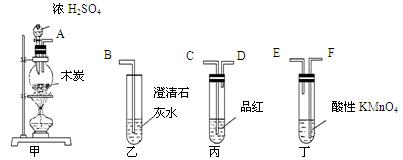
(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):
接 , 接 , 接 ;
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?
乙中 ____ ,丙中 ______ ;
(3)丁中酸性KMnO4溶液的作用是 ;
(4)写出甲中反应的化学方程式 ______ 。
查看答案和解析>>
科目: 来源: 题型:
下列事故或药品的处理正确的是
A.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
B.有大量氯气泄漏,逃生时可以用肥皂水(碱性)浸湿毛巾捂住嘴和鼻
C.不慎洒出的酒精在桌上燃烧起来,应立即用大量水扑灭
D.将含硫酸的废液倒入水槽,用水冲入下水道
查看答案和解析>>
科目: 来源: 题型:
在下列变化①大气固氮 ②硝酸分解 ③实验室制取氨气中,按氮元素被氧化、被还原、既不被氧化又不被还原的顺序排列,正确的是
A.①②③ B.②①③ C.③②① D.③①②
查看答案和解析>>
科目: 来源: 题型:
下列关于铜电极的叙述中不正确的是
A.在镀件上镀铜时可用金属铜作阳极 B.锌铜原电池中铜是正极
C.用电解法精炼粗铜时纯铜作阳极 D.用电解法精炼粗铜时粗铜作阳极
查看答案和解析>>
科目: 来源: 题型:
关于下列装置说法正确的是( )
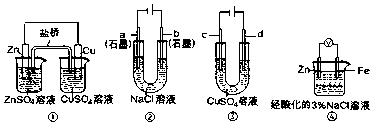
A.用装置③精炼铜时,c极为粗铜
B.装置①中,盐桥中的K+移向ZnSO4溶液
C.装置②工作一段时间后,a极附近溶液的pH增大
D.装置④中电子由Zn流向Fe,装置中有Fe2+生成
查看答案和解析>>
科目: 来源: 题型:
常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题意回答下列问题:
(1)写出酸H2A的电离方程式__________________________。
(2)若溶液M由10mL 2 mol·L-1NaHA溶液与10mL 2mol·L-1NaOH溶液混合而得,则溶液M的pH ________7 (填“>”、“<”或“=”),溶液中离子浓度由大到小顺序为 。已知Ksp(BaA)= 1.8×10-10,向该混合溶液中加入10mL 1 mol·L-1 BaCl2溶液,混合后溶液中的Ba2+浓度为___________ mol·L-1。
(3)若溶液M由下列三种情况:①0.01mol·L-1的H2A溶液②0.01mol·L-1的NaHA溶液③0.02mol·L-1的HCl与0.04mol·L-1的NaHA溶液等体积混合液,则三种情况的溶液中H2A分子浓度最大的为_______ ;pH由大到小的顺序为_________________ 。
(4)若溶液M由pH=3的H2A溶液V1 mL与pH=11的NaOH溶液V2 mL混合反应而得,混合溶液c(H+)/c(OH-)=104,V1与V2的大小关系为___________(填“大于、等于、小于”或“均有可能”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com