
科目: 来源: 题型:
下列化工生产过程中所发生的主要化学反应不属于氧化还原反应的是
A.用氯气和消石灰制漂白粉 B.铝热法冶炼金属钒
C.用石灰石、纯碱、二氧化硅制玻璃 D.电解饱和食盐水制烧碱
查看答案和解析>>
科目: 来源: 题型:
可逆反应A(气)+B(气)![]() 3C(气),下图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
3C(气),下图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
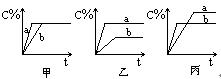
(1)若甲图中两条曲线分别表示有催化剂和无催化剂时的情况,则___ 曲线是表示有催化剂时的情况。
(2)若乙图中的a曲线表示200℃和b曲线表示100℃时的情况,则此可逆反应的正反应是_____ 热反应。
(3)若丙图中两条曲线分别表示不同压强下的情况,则____ 曲线是表示压强较大的情况。
查看答案和解析>>
科目: 来源: 题型:
酸雨给人类带来了种种灾祸,严重地威胁着地球生命生存的生态环境,下列有关减少或者防止酸雨形成的措施中可行的是:①对燃煤进行脱硫;②对含SO2、NO2等工业废气进行无害处理后,再排放到大气中;③人工收集雷电作用所产生的氮的氧化物;④飞机、汽车等交通工具采用清洁燃料,如天然气、甲醇等。
A.①②③④ B.①②③ C.①②④ D.①③④
查看答案和解析>>
科目: 来源: 题型:
下列反应的离子方程式正确的是( )
A.硫酸镁溶液跟氢氧化钡溶液反应:![]() +Ba2+=BaSO4↓
+Ba2+=BaSO4↓
B.稀硫酸滴在铜片上: Cu+2H+=Cu2++H2↑
C.FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
D.食醋除水垢中的碳酸钙:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑
查看答案和解析>>
科目: 来源: 题型:
短周期元素X、Y、Z和W 的原子序数依次递增,且在同一周期,四种元素原子的最外层电子数之和为19, X和Y元素原子的原子序数比6∶7,X的最高正价是W的最低负价的绝对值的2倍。下列说法正确的是( )
A.X单质可以通过铝热法获得
B.Y的氧化物是良好的半导体材料
C.Z的氢化物比W的氢化物更稳定
D.X的最高价氧化物和Z的最高价氧化物化合的产物中有共价键和离子键
查看答案和解析>>
科目: 来源: 题型:
多晶硅(硅单质的一种)被称为“微电子大厦的基石”,制备中副产物以SiCl4为主,它对环境污染很大,能遇水强烈水解,放出大量的热。研究人员利用SiCl4水解生成的盐酸和钡矿粉(主要成份为BaCO3,且含有钙、铁、镁等离子)制备BaCl2·2H2O,工艺流程如下。已知常温下Fe3+、Mg2+完全沉淀的pH分别是:3.4、12.4。 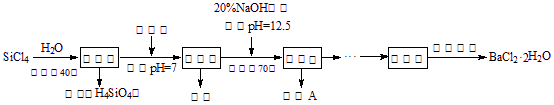
(1)SiCl4水解控制在40℃以下的原因是 ▲ 。
已知:SiCl4(s)+H2(g)=SiHCl3(s)+HCl(g) ΔH1=47 kJ/mol
SiHCl3(s)+H2(g)=Si(s)+3HCl(g) ΔH2=189 kJ/mol
则由SiCl4制备硅的热化学方程式为 ▲ 。
(2)加钡矿粉时生成BaCl2的离子反应方程式是 ▲ 。
(3)加20% NaOH调节pH=12.5,得到滤渣A的主要成分是 ▲ ,控制温度70℃的目的是 ▲ 。
(4)BaCl2滤液经蒸发浓缩、降温结晶、过滤,再经真空干燥后得到·2H2O。实验室中蒸发浓缩用到的含硅酸盐的仪器有 ▲ 种。
(5)为体现该工艺的绿色化学思想,该工艺中能循环利用的物质是 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
在等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中,下列式子表达可能不正确的是
A. c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-)
![]() B. c(Na+)+ c(H+)=c(X-)+c(OH-)
B. c(Na+)+ c(H+)=c(X-)+c(OH-)
![]() C.
C.
D.
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是
A.合成氨生产中将NH3液化分离,可加快正反应速率,提高H2的转化率
B.硫酸工业中,接触室中热交换器是利用SO3转化为H2SO4时放出的热量
C.氯碱工业采用离子交换膜法,可防止阳极室产生的Cl2进入阴极室
D.钢铁发生吸氧腐蚀时,阴极的反应式为:Fe-2e→Fe2+
查看答案和解析>>
科目: 来源: 题型:
有a、b、c、d四种金属,将a与b用导线连结起来浸入电解质溶液中,b不易腐蚀;将a、d分别投入等浓度的盐酸中,d比a反应剧烈;将Cu浸入b的盐溶液里,无明显变化;如果把Cu浸入c的盐溶液里,有c的单质析出.据此判断它们的活动性由强到弱的顺序是( )
A.d、c、a、b B.d、a、b、c C.d、b、a、c D.b、a、d、c
查看答案和解析>>
科目: 来源: 题型:
可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是( )
A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O2+2H2O+4e-=4OH-
B.以NaOH溶液为电解液时,负极反应为:Al+3OH--3e-=Al(OH)3↓
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com