
科目: 来源: 题型:
在用锌片、铜片和稀硫酸组成的原电池装置中,经过—段时间工作后,下列说法正确的是
A.锌片是正极,铜片是负极 B.电子是从锌片通过导线流到铜片上
C.溶液中H+移向锌片被还原成H2 D.电解液的pH逐渐变小
查看答案和解析>>
科目: 来源: 题型:
高纯碳酸锰广泛应用于电子工业,是制造高性能磁性材料的主要原料。新工艺采用工业冶铜后的废气SO2进行湿法浸取软锰矿(主要含MnO2,同时含有少量SiO2、Fe2O3、Al2O3)来制备。(已知亚硫酸酸性强于碳酸)
①将过量的SO2气体通入软锰矿浆中进行“浸锰”操作,并控制温度加热反应;
②向浸锰结束后的滤液中加入MnO2、同时通入空气,再用Na2CO3溶液调节pH为3.7后
过滤分离;
③调节滤液pH值为6.5~7.2 ,然后加入NH4HCO3 ,有浅红色的沉淀生成,过滤洗涤干燥后就可以得到高纯碳酸锰。
工业流程图如下:
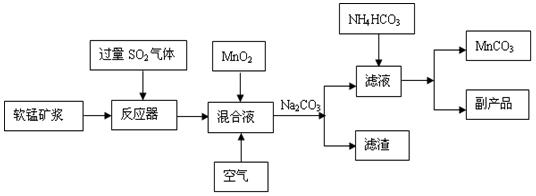
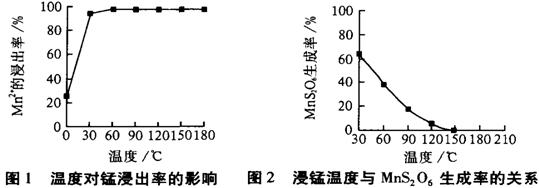
已知生成氢氧化物的pH如下表:
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 |
查看答案和解析>>
科目: 来源: 题型:
某课外活动小组研究金属钾的性质。他们通过Na、K原子结构示意图及查找有关资料,知道了Na、K属于同一类物质,且K燃烧生成KO2。请完成下列内容:
(1)观察钾的切面。硬度: ,颜色:
(2)预测钾的性质,并进行实验验证(用化学方程式表示):
①在空气中缓慢氧化: ;
②点燃,发生剧烈燃烧: ;
③与水剧烈反应: 。
(3)结论:钾是一种活泼的金属单质,其化学性质比钠活泼。
(4)该小组研究钾的性质用到了哪几种方法。
答: 。
查看答案和解析>>
科目: 来源: 题型:
某无色溶液X,由Na+、Ag+、Ba2+、Al3+、AlO2-、MnO4-、CO32-、SO42-中的若干种离子组成,取溶液进行如下连续实验:
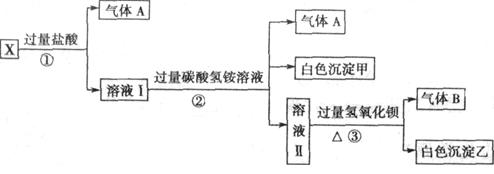
(1)白色沉淀甲是 _________。
(2)X溶液中一定存在的离子是_____________。
(3)白色沉淀乙中一定有:______,可能有_______ 证明其是否存在的方法是______________。
(4)若将过量的气体A与适量的气体B通入水中,写出反应的离子方程式_____________。
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式正确的是( )
A.碳酸氢钠溶液与少量石灰水反应 HCO3-+ Ca2+ + OH- = CaCO3↓ + H2O
B.铁溶于稀硝酸,溶液变黄: Fe+4H++ NO3-=== Fe3++ NO↑+2H2O
C.Na2CO3溶液显碱性:CO32-+H2O=== HCO3-+OH-
D.已知稀溶液中,酸碱反应的中和热为57.3KJ/mol,则将浓度均为0.1mol/l的NaOH溶液与醋酸等体积混合时的热化学方程式为:
NaOH(aq)+CH3COOH(aq)===CH3COONa(aq)+H2O(l);△H=-57.3kJ/mol
查看答案和解析>>
科目: 来源: 题型:
有甲、乙、丙三种试液。在氢氧化钡溶液中加入甲,有白色沉淀生成;在沉淀中加入乙,沉淀溶解并产生气泡;最后加入丙,又产生白色沉淀。则试液甲、乙、 丙依次是
A. Na2CO3、HNO3、MgSO4 B. Na2CO3、HCl、CaCl2
C. H2SO4、(NH4)2CO3、AgNO3 D. Na2SO3、Na2CO3、MgSO4
查看答案和解析>>
科目: 来源: 题型:
向含0.78molFeCl2溶液中通入0.09molCl2, 再加入100mL1mol/L的X2O72-酸性溶液,使溶液中的Fe2+恰好全部氧化,则产物中X的化合价为
A.+1 B.+2 C.+3 D.+5
查看答案和解析>>
科目: 来源: 题型:
某氧化剂中,起氧化作用的是X2O72-离子,在溶液中0.2mol该离子恰好能使0.6mol的SO32-离子完全氧化,则X2O72-离子还原后X的化合价为( )
A. +1 B. +2 C. +3 D. +4
查看答案和解析>>
科目: 来源: 题型:
反应CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH=-41.2kJ·mol-1,在800℃时的化学平衡常数K=1.0。某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
CO2(g)+H2(g) ΔH=-41.2kJ·mol-1,在800℃时的化学平衡常数K=1.0。某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
| CO | H2O | CO2 | H2 |
| 0.5 mol | 8.5 mol | 2.0 mol | 2.0 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com