
科目: 来源: 题型:
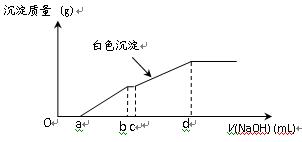
向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如下图,则原混合溶液中MgCl2与FeCl3的物质的量之比为
A.![]() B.
B.![]()
C.![]() D.
D.![]()
查看答案和解析>>
科目: 来源: 题型:
下列实验或操作能达到预期目的的是
①用溴水鉴别苯、乙醇、溴苯
②用盐酸酸化的硝酸钡溶液鉴别硫酸根离子与亚硫酸根离子
③用食醋和澄清石灰水验证蛋壳中含有碳酸盐
④将碘水倒入分液漏斗,加入CCl4,振荡后静置,可将碘萃取到CCl4中
⑤在容量瓶中加入一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸
A.①②③ B.①③④ C.②③④ D.②④⑤
查看答案和解析>>
科目: 来源: 题型:
已知a、b分别为ⅠA和ⅦA族的同周期两种元素,它们的原子序数分别为m和n,则下列关系不可能成立的是( )
A. n=m+6 B. n=m+16 C. n=m+30 D. n=m+10
查看答案和解析>>
科目: 来源: 题型:
氯化亚铜(CuCl)是白色粉末,不溶于水、乙醇,熔点422℃,沸点1366℃,在空气中迅速被氧化成绿色,常用作有机合成工业中的催化剂。以粗盐水(含Ca2+、Mg2+、SO2-4等杂质)。Cu、稀硫酸,SO2等为原料合成CuCl的工艺如下:
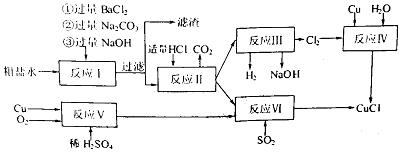
(1)反应I中加Na2CO3溶液的作用是 。
过一步反(2)反应II在电解条件下进行,电解时阳极发生的电极反应可表示为 。
(3)写出反应VI的化学方程式 。
(4)反应IV加入的Cu必须过量,其目的是 。
(5)反应VI后,过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却,密封包装即得产品。于70℃真空干燥的目的是 。
查看答案和解析>>
科目: 来源: 题型:
a、b、c、d、e是同周期的五种元素, a的最高价氧化物对应水化物的碱性弱于b的; c的气态氢化物的还原性弱于d的;五种元素的原子得到或失去电子后所形成的简单离子中,e的离子半径最小,则它们的原子序数由小到大的顺序是
A、abdce B、baedc C、ebadc D、cdeab
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是
A.久置的浓HNO3呈黄色,为除去黄色可通入O2
B. NH4Cl4固体中混有I2,可用加热的方法除去
C.为除去FeSO4溶液中的Fe2(SO4)3 可加入Cu 粉
D.为除去SO2中少量的CO2,可使其通过澄清石灰水
查看答案和解析>>
科目: 来源: 题型:阅读理解
(1)下列实验操作或叙述正确的是 (填写编号,多选扣分)
①不宜用瓷坩埚灼烧氢氧化钠或碳酸钠固体;
②为了提高纯锌与稀硫酸反应的速率,可向稀硫酸中滴入几滴![]() 溶液;
溶液;
③用蒸馏水润湿的pH试纸测定溶液的pH一定有误差;
④向沸腾的NaOH稀溶液中滴加![]() 饱和溶液,可以制得
饱和溶液,可以制得![]() 胶体;
胶体;
⑤配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸;
⑥定容时,俯视容量瓶刻度,造成所配溶液浓度偏高;
⑦称取5.85g 氯化钠固体,用100 mL蒸馏水溶解,得到1.00 mol·L-1 氯化钠溶液
(2)某钠盐溶液可能含有阴离子NO3-,CO32-,SO32-,SO42-,Cl-,Br-,I-。为鉴定这些离子,分别取少量溶液进行以下各步骤的实验:
步骤1测得混合液呈碱性;
步骤2滴加HCl时,溶液中出现气泡。该气体能使饱和石灰水溶液变浑浊;
![]() 步骤3加CCl4,滴加少量氯水,振荡后,CCl4层未变色;
步骤3加CCl4,滴加少量氯水,振荡后,CCl4层未变色;
步骤4加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
步骤5加HNO3酸化后,再加过量AgNO3,溶液中析出白色沉淀。
分析上述5个实验,回答下列问题。
①由实验步骤1判断可能存在的离子有 ;
②由实验步骤2判断可能存在的离子有几种可能性 ;分别是 ;
③由实验步骤3可得出的结论是 ;
④由实验步骤4和实验步骤5可确定肯定存在的离子有 ;
⑤由上述5个实验不能确定是否存在的离子是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com