
科目: 来源: 题型:
1mol液态有机物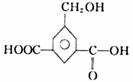 分别与足量Na、CH3COOH溶液、NaOH溶液反应,消耗三种药品的物质的量之比为( )
分别与足量Na、CH3COOH溶液、NaOH溶液反应,消耗三种药品的物质的量之比为( )
A.3:2:1 B.3:1:1 C.3:1:2 D.2:3:1
查看答案和解析>>
科目: 来源: 题型:
下表是元素周期表的一部分,完成以下有关问题。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)在①~⑩元素中,最不活泼的元素是_____(写元素符号,下同);最高价氧化物对应的水化物的酸性最强的元素是 ,最高价氧化物对应的水化物的碱性最强的元素是 。
(2)②、③、④的氢化物中最稳定是 (填该氢化物化学式)。
(3)④⑤⑥的原子半径从大到小的顺序是 > > (写元素符号) 。
(4)①的一种氢化物的产量是衡量一个国家石油化学工业发展水平的标志,该氢化物与⑨的氢化物反应的化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
在测定中和热的实验中,下列说法中正确的是 ( )
A.该实验需要用的主要玻璃仪器有:两个大小相同的烧杯、两只大小相同的量筒、温度计、环形玻璃搅拌棒
B.不能用保温杯代替烧杯做有关测定中和热的实验
C.该实验至少需要测定并记录温度的次数是6次
D.若NaOH的物质的量稍大于HCl,会导致所测中和热数值偏高
查看答案和解析>>
科目: 来源: 题型:阅读理解
氨气是一种重要工作原料,在工农业生产中具有重要的应用。
(1)已知:N2(g)+O2(g)=2NO(g) △ H=180.5kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-905 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1
则N2(g)+3H2(g)=2NH3(g)的△H=_________________________。
(2)工业合成氨气的反应为N2(g)+3H2(g) ![]() 2NH3(g)。在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是_________ _________。
2NH3(g)。在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是_________ _________。
①增大压强 ②增大反应物的浓度 ③使用催化荆 ④降低温度
( 3 )①实验室常用加热氯化铵固体和氢氧化钙固体的混合物来制取氨气,写出反应的化学方程式 ?? 。实验室还可在 ?? (填一种试剂)中滴加浓氨水的方法快速制取少量氨气。
② 常温下氨气极易溶于水,溶液可以导电。氨水中水电离出的c(OH-) 10-7 mol·L-1(填写“>”、“<”或“=”);
③ 将相同体积、PH之和为14的氨水和盐酸混合后,溶液中离子浓度由大到小的顺序
为 。
(4)合成氨的原料氢气是一种新型的绿色能源,具有广阔的发展前景。现用氢氧燃料电池进行图所示实验:(其中a、b均为碳棒)
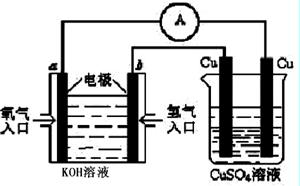
①氢氧燃料电池具有广阔的发展前景。如下图所示:
右边Cu电极反应式是 。
a电极的电极反应式
②工业上生产氢气是将水蒸气通过红热的炭,产生水煤气:
C(s) + H2O(g) ![]() H2(g) + CO(g) △H = +131.3 kJ/mol
H2(g) + CO(g) △H = +131.3 kJ/mol
该反应在低温下不能自发进行的原因是 。
A.△H >0 B.温度较低时,△H影响为主
C.△ S<0 D.温度较低时,△S影响为主
查看答案和解析>>
科目: 来源: 题型:
如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )
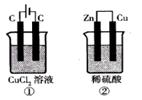
A.产生气体的体积:①>②
B.溶液的pH变化:①增大 ②不变
C.电极上析出物质的质量:①>②
D.电极反应式:①中阳极 ![]() ②中负极
②中负极 ![]()
查看答案和解析>>
科目: 来源: 题型:
进行胃部透视时,常在检查之前服用“钡餐”,其主要成分是硫酸钡。
(1)25℃时,已知胃液的pH在0.9—1.5之间,请问___ (填“能”或“不能”)用
碳酸钡代替硫酸钡作为“钡餐”使用,简述你做出判断的理由:_
。
(2)当人体中Ba2+浓度达到2×10-3mol·L-1时,就会对健康产生危害,若误将氯化钡当做食盐使用,请计算说明是否可以通过服用5%的硫酸钠溶液(约0.36mol·L-1)有效除去胃中的Ba2+。(25℃时,硫酸钡的溶度积常数Ksp=1.1×10-10)
。
![]() (3)环境监测某工厂废水中Ba2+的浓度。取废水50.00mL,控制适当的酸度加入足量的K2Cr2O7溶液,得BaCrO4沉淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO42-全部转化为Cr2O72-,再加入过量KI溶液,反应液中再滴加0.100mol·L-1Na2S2O3溶液,反应完全时,消耗Na2S2O3溶液36.00mL。已知有关的离子方程式为:
(3)环境监测某工厂废水中Ba2+的浓度。取废水50.00mL,控制适当的酸度加入足量的K2Cr2O7溶液,得BaCrO4沉淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO42-全部转化为Cr2O72-,再加入过量KI溶液,反应液中再滴加0.100mol·L-1Na2S2O3溶液,反应完全时,消耗Na2S2O3溶液36.00mL。已知有关的离子方程式为:
① Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O;② I2+2S2O32-=2I-+S4O62-。
试计算该工厂废水中Ba2+的物质的量浓度。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com