
科目: 来源: 题型:
某草酸亚铁样品中含有少量硫酸亚铁。现用滴定法测定该样品中FeC2O4的含量。滴定反应是:5 Fe2+ +5C2O42—+3MnO4—+24H+==5 Fe3+ +10CO2↑+3Mn2++12H2O。
实验方案设计为:
①将准确称量的a g草酸亚铁样品置于250 mL锥形瓶内,加入适量2 mol/L的H2SO4溶液,使样品溶解,加热至70℃左右,立即用浓度为0.02000 mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为b ml。
②向上述滴定混合液中加入适量的Zn粉和过量的2 mol/L的H2SO4溶液,煮沸5—8min,经检验溶液合格后(不含Fe3+),继续用0.02000 mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为c ml。
③ 。
④数据处理。
请回答下列问题:
⑴上述实验方案中的步骤③是 ▲ 。
⑵洁净的滴定管在滴定前必须进行的操作是:
Ⅰ、 ▲ ;
Ⅱ、用高锰酸钾标准溶液润洗滴定管;
Ⅲ、加入高锰酸钾标准溶液,赶走尖嘴部位的气泡;
Ⅳ、 ▲ 。
⑶步骤②中检验溶液是否合格的操作是:取1滴煮沸后的溶液滴入装有 ▲ 溶液的试管中,如 ▲ ,则说明溶液合格。
⑷某实验探究小组的一次测定数据记录如下:
| a/g | 起始读数/mL | b/mL | c/mL |
| 0.1582 | 0.00 | 29.90 | 40.90 |
| 0.1582 | 0.00 | 30.10 | 41.10 |
| 0.1582 | 0.00 | 32.10 | 43.10 |
根据数据计算0.1582g 样品中:n(Fe2+)= ▲ ; n(C2O42—)= ▲ ;
FeC2O4(FeC2O4 的摩尔质量为144g/mol)的质量分数为 ▲ 。(精确到0.1%)
查看答案和解析>>
科目: 来源: 题型:
关于下列各装置图的叙述中,正确的是
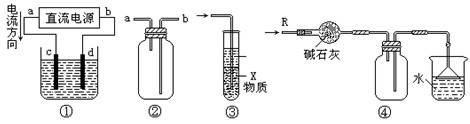
A.①中,d极发生氧化反应、c极发生还原反应
B.②中从a口通入气体,可用于收集H2、NH3、CH4等气体
C.③中X若为CCl4,上层为稀硫酸,可用于吸收氨气,并防止倒吸
D. ④可用于干燥、收集氯化氢,并吸收多余的氯化氢
查看答案和解析>>
科目: 来源: 题型:
在光照条件下,将1 mol CH4与1 mol Cl2混合充分反应后,得到的产物是
A、CH3Cl HCl B、CCl4 HCl
C、CH3Cl CH2Cl2 D、CH3Cl CH2Cl2 CHCl3 CCl4 HCl
查看答案和解析>>
科目: 来源: 题型:
下列各组在溶液中反应,不管反应物的量是多少,都能用同一离子方程式表示的是( )
A.FeBr2与Cl2 B.Ba(OH)2与H2SO4
C.HCl与Na2CO3 D.NaHCO3与Ca(OH)2
查看答案和解析>>
科目: 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.100 mL pH=2的盐酸与醋酸溶液中氢离子数均为10-3NA
B.标准状况下,11.2 L C2H2和N2的混合气分子中σ键数目为0.5NA
C.常温常压下,4.6 g Na在O2中燃烧消耗O2的分子数为0.05NA
D.常温常压下,33.6 L氯气与27 g铝充分反应,转移电子数为3NA
查看答案和解析>>
科目: 来源: 题型:
已知某工业废水中含有CuCl2、FeCl2、HCl,某化学探究学习小组打算用这种废水制备纯净的FeCl2晶体。为此他们设计了如下的实验方案:
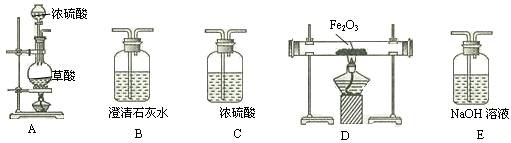
第一步:用上图中的仪器和药品组装一套实验装置制取干燥的CO,用CO还原Fe2O3粉末制取还原铁粉。提示:制取CO的原理为![]() 。
。
(1)如果所制气体流向从左向右时,上述组装的实验装置从左向右的实验装置连接顺序(填仪器序号)是 ![]()
![]()
![]()
![]() 。
。
(2)正确的操作第一步应是 ;最后一步应是熄灭 处的酒精灯。
(3)装置B的作用是 ;装置E的作用是 。
(4)第二步:将制得的还原铁粉放入原混合溶液中,制得纯净的FeCl2溶液。
必须进行的操作是 。
(5)第三步:得到纯净的FeCl2晶体。
必须进行的操作是 。
查看答案和解析>>
科目: 来源: 题型:
某离子晶体晶胞结构如下图所示,X位于立方体的顶点,Y位于立方体中心。
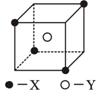
试分析:
(1)晶体中每个Y同时吸引着__________个X,每个X同时吸引着__________个Y,该晶体的化学式为 。
(2)晶体中在每个X周围与它最接近且距离相等的X共有_________________个。
(3)晶体中距离最近的2个X与1个Y形成的夹角∠XYX的度数为__________。
(4)设该晶体的摩尔质量为M g·mol-1,晶体密度为ρg·cm-3,阿伏加德罗常数为NA mol-1,计算此晶体中两个距离最近的X中心间的距离______________________cm。
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是
A.干冰升华时分子内共价键会发生断裂
B.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性
C.分子晶体的熔沸点低,常温下均呈液态或气态
D.金属导电的原因是在外加电场的作用下金属产生自由电子,电子定向运动
查看答案和解析>>
科目: 来源: 题型:
某化学兴趣小组用铜和浓硫酸制取SO2,并检验SO2的性质,实验装置如下图所示:
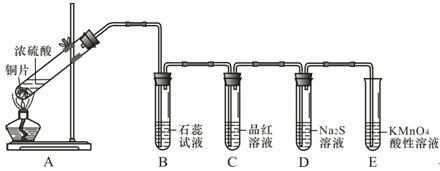
已知,酸性KMnO4溶液具有强氧化性,许多气体能够使酸性KMnO4溶液褪色。
请回答下列问题:
(1)装置A的试管中发生反应的化学方程式是 。
(2)装置B中的现象是 ,装置D中的现象是 。
(3)分析实验意图,装置C证明SO2具有 性,装置E能够起到的两个作用是 、 。
(4)实验过程中还观察到A试管内产生黑色沉淀,黑色沉淀是副反应产物,可能是CuO、CuS和Cu2S。已知CuS和Cu2S均不溶于盐酸、硫酸。如何用化学方法证明黑色沉淀中没有CuO ? 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com