
科目: 来源: 题型:
现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若用nA 代表阿伏加德罗常数的数值,则:(只要求写出结果)
(1)该气体的物质的量为________mol。(2)该气体在标准状况下的体积为_________L。
(3)该气体所含原子总数为_______ 个。
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为___ _。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为_____ mol/L。
查看答案和解析>>
科目: 来源: 题型:
24mL 0.05mol/L的Na2SO3溶液,恰好与20mL0.02mol/L的K2Cr2O7溶液完全反应,Na2SO3生成Na2SO4,则铬元素在还原产物中的化合价为( )
A. +6 B. +2 C. +3 D. 0
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏加德罗常数,下列说法中正确的是 ( )
A.1000mL0.1mol/L 的NaCl溶液中,Na+与Cl-离子总数为0.2NA
B.2NA个二氧化碳分子的质量为44g
C.NA个氢气分子所占的体积为22.4L
D.17g氨气中所含原子数为NA
查看答案和解析>>
科目: 来源: 题型:
在雷达的微波过滤器里使用的铁氧磁性体,如钇铁石榴石Y3Fe5O12,其中Y是ⅢB族稀土元素。下面有关钇铁石榴石的叙述中正确的是
A、可表示为3YO3·3FeO·Fe2O3 B、可表示为Y3O5·Fe3O4·Fe2O3
C、其中钇、铁的化合价均为+3价 D、其中钇、铁的化合价均有+2、+3价
查看答案和解析>>
科目: 来源: 题型:
2004年7月德俄两国化学家共同宣布,在高压下氮气会聚合生成高聚氮,这种高聚氮的 晶体中每个氮原子都通过三个单键与其它氮原子结合并向空间发展构成立体网状结构。已知晶体中N-N键的键能为160 kJ·mol-1,而N≡N的键能为942 kJ·mol-1(键能表示形成化学键释放的能量或者破坏化学键消耗的能量)。则下列有关说法不正确的是
A.键能越大说明化学键越牢固,所构成物质越稳定
B.高聚氮晶体属于原子晶体
C.高聚氮晶体中n(N)∶n(N-N)=1∶3
D.用作炸药或高能材料可能是高聚氮潜在的应用
查看答案和解析>>
科目: 来源: 题型:
实现化学实验绿色化的要求,有效地减少污染,可把化学实验设计成微型化。某研究性学习小组的学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1 mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即用表面皿盖好。
(1)在a处观察到的实验现象:_____________________________________。
在c处观察到的实验现象:______________________________________。
(2)e处反应的离子方程式为___________________________________。
该反应中氧化剂和还原剂的物质的量之比为__________________________。
(3) d处反应所产生的现象为___ _______________。
标准状况下,当有0.112 L Cl2被NaOH溶液吸收后,转移电子为________mol。
(4)通过该实验能否比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱?________(填“能”或“不能”),若能,其氧化性由强到弱的顺序是____________ ___。
查看答案和解析>>
科目: 来源: 题型:
![]() 反应过程的能量变化如图所示。已知
反应过程的能量变化如图所示。已知![]() 氧化为
氧化为![]() 的
的![]() 。请回答问题:
。请回答问题:
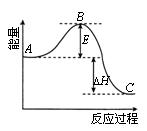
(1)图中A、C分别表示 、 ,E的大小对该反应的
反应热有无影响? 。该反应通常用![]() 作催化剂,加
作催化剂,加![]() 会使图中
会使图中
B点升高还是降低? ,理由是 。
(2)图中![]()
![]() 。
。
(3)![]() 的催化循环机理可能为:
的催化循环机理可能为:![]() 氧化
氧化![]() 时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式 。
时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式 。
(4)如果反应速率![]() 为
为![]() ,则
,则![]()
![]() 、
、![]()
![]() 。
。
(5)已知单质硫的燃烧热为![]() ,计算由
,计算由![]() 生成
生成![]() 的
的![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
短周期元素![]() 的原子序数依次递增,其原子的最外层电子数之和为11;
的原子序数依次递增,其原子的最外层电子数之和为11;![]() 在同一周期;Z原子最外层电子数是X原子内层电子数的2倍,也是Y原子最外层电子数的2倍。下列说法中,正确的是( )
在同一周期;Z原子最外层电子数是X原子内层电子数的2倍,也是Y原子最外层电子数的2倍。下列说法中,正确的是( )
A.离子半径:![]() B.气态氢化物的稳定性:
B.气态氢化物的稳定性:![]()
C.![]() 的氧化物中含有离子键 D.
的氧化物中含有离子键 D.![]() 的氧化物对应的水化物是弱碱
的氧化物对应的水化物是弱碱
查看答案和解析>>
科目: 来源: 题型:
氮气和氢气的混合气体在放电时只生成少量的氨,但如果在混合气体下面放有硫酸,这个反应几乎可以进行到底,主要原因是
A.硫酸起了催化剂的作用
B.硫酸起了脱水剂的作用
C.硫酸吸收了氨,增大了正反应速率
D. 硫酸吸收了氨,减小了逆反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com