
科目: 来源: 题型:
下列说法正确的是
A.根据丁达尔现象可以区分食盐水和硫酸铜溶液
B.某离子被沉淀完全是指该离子在溶液中的浓度等于0
C.在任何条件下,纯水都呈中性
D.水的离子积常数Kw随温度、外加酸(碱)浓度的改变而改变
查看答案和解析>>
科目: 来源: 题型:
工业上制备纯硅反应的热化学方程式如下: SiCl4(g)+2H2(g) =Si(s)+4HCl(g)
ΔH=+Q kJ·mol-1 (Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ
C.反应至4 min时,若HCl浓度为0.12 mol·L-1,则H2的反应速率为0.03 mol/(L·min)
D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol·L-1的NaOH溶液恰好反应
查看答案和解析>>
科目: 来源: 题型:
七水硫酸镁(MgSO4·7H2O)在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣-硼镁泥可制取七水硫酸镁。硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等)。
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 |
表2 两种盐的溶解度(单位为g/100g水)
| 温度 / ℃ | 10 | 30 | 40 | 50 | 60 |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
| MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 | / |
硼镁泥制取七水硫酸镁的工艺流程如下:
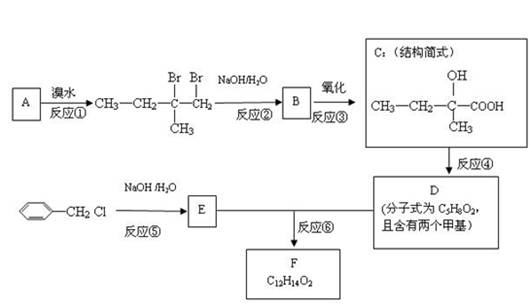
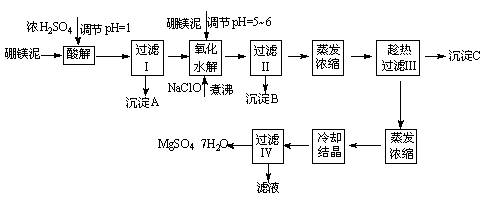
根据以上流程图并参考表格pH数据和溶解度数据,试回答下列问题:
(1)过滤I的滤液中加入硼镁泥,调节溶液的pH=5~6,再加入NaClO溶液加热煮沸,将溶液中的Mn2+氧化成MnO2,反应的离子反应方程式为 。加热煮沸的主要目的是_ 。 (2)沉淀B中除MnO2、SiO2外还含有 (填化学式)等物质。
(3)检验过滤Ⅱ后的滤液中是否含有Fe3+的实验方法是 ;
(4)沉淀C的化学式是 。过滤III需趁热过滤的理由是 。
查看答案和解析>>
科目: 来源: 题型:
下列溶液中氯离子的物质的量浓度与50mL1mol·L-1氯化铝溶液中氯离子的物质的量浓度相等的是
A.150mL1mol·L-1氯化钠溶液 B. 75mL2mol·L-1氯化铵溶液
C.150mL3mol·L-1氯化钾溶液 D. 50 mL3mol·L-1氯化亚铁溶液
查看答案和解析>>
科目: 来源: 题型:
下列热化学方程式中 ΔH的数值能表示可燃烧热的是
A.H2(g) + Cl2(g) = 2HCl(g) ΔH =-184.6kJ/mol
B.CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) ΔH =-802.3kJ/mol
C.2H2(g) + O2(g) = 2H2O(l) ΔH =-571.6kJ/mol
D.CO(g) + 1/2O2(g) = CO2(g) ΔH =-283kJ/mol
查看答案和解析>>
科目: 来源: 题型:阅读理解
已知A、B为常见的金属单质,C、D为常见的非金属单质,甲、乙、丙为三种常见的化合物,甲是中学化学中常见的红棕色粉末状固体,它们之间的相互转化关系如图所示(部分产物及反应条件没有列出):
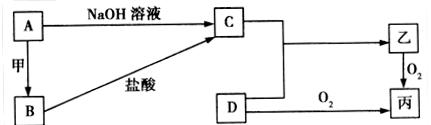
(1)写出框图中A转化为B的化学方程式:_______________________________________,该反应属于______________(填“吸热反应”或“放热反应”)。
(2)若乙的水溶液呈弱酸性,丙是一种大气污染物、有刺激性气味。已知16 g固体单质D完全燃烧转化成丙时,放出148.4 kJ的热量,则该反应的热化学方程式为:
_____________________________________________________________________________。
(3)若乙在水溶液中呈弱碱性,其盐可用作化肥,且C与D化合生成乙的反应是可逆反应。
①将等物质的量的C、D两种单质充入一体积恒定的密闭容器中,在适当催化剂和恒温条件下反应,下列说法中不正确的是____________(填字母)。
a.达到化学平衡时,2υ正(C) = 3υ逆(乙)
b.反应过程中,D单质的体积分数始终为50%
c.达到化学平衡时,混合气体的密度保持不变
d.达到化学平衡的过程中,气体的平均相对分子质量逐渐增大
e.达到化学平衡后,再升高温度,乙的体积分数增大
②若在一个体积为10 L的密闭容器中,充入8 mol C单质和2 mol D单质,在一定温度下发生反应生成气体乙,经40 min后反应达到平衡,此时C的转化率为37.5%。从反应开始到达平衡的40 min内,用物质乙表示的化学反应速率为_________________________;达到平衡后,若向容器中按5∶1∶2的物质的量之比再次充入C、D、乙三种物质,则原平衡体系中C的转化率将_____________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
在1 L mol![]() L—1的氨水中( )
L—1的氨水中( )
A.含有1molNH3分子 B.含NH3和NH4+之和为1mol
C.含![]() 1mol D.含NH3、
1mol D.含NH3、![]() 、NH4+之和为1mol
、NH4+之和为1mol
查看答案和解析>>
科目: 来源: 题型:
下列有关金属及其化合物的说法正确的是( )
A.由于铝在常温下不能与氧气反应,所以铝制品具有一定的抗腐蚀性能,是一种应用
广泛的金属材料
B.住FeCl3溶液中滴入KI一淀粉溶液,溶液变蓝色
C.向紫色石蕊试液中加入过量的Na2O2粉末,振荡,溶液变为蓝色并有气泡产生
D.装修门窗使用的铝合金材料的硬度比铝小,熔点比铝低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com