
科目: 来源: 题型:
设NA为阿伏加德罗常数,下列对0.3mol/LK2SO4溶液的不正确说法是( )。
A.1L溶液中含有0.3NA个K+离子
B.1L溶液中含有K+和SO42-离子总数为0.9NA
C.2L溶液中含K+的物质的量浓度为1.2mol/L
D. 2L溶液中含0.6NA个SO42-离子
查看答案和解析>>
科目: 来源: 题型:
下列热化学方程式或离子方程式中,正确的是:
A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:有CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:
![]() △H=-38.6kJ·mol-1
△H=-38.6kJ·mol-1
C. 氯化镁溶液与氨水反应:![]()
D. 氧化铝溶于NaOH溶液:![]()
查看答案和解析>>
科目: 来源: 题型:
某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是_______________。
(2)该反应中,发生还原反应的过程是 → 。
(3)该反应中氧化剂与还原剂物质的量之比为 。
(4)如反应转移了0. 3mol电子,则产生的气体在标准状况下体积为 。
查看答案和解析>>
科目: 来源: 题型:
373K时,某 1L密闭容器中加入1molPCl5发生如下可逆反应:![]() 其中物质PCl3的物质的量变化如右图所示。
其中物质PCl3的物质的量变化如右图所示。
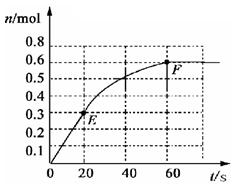
(1)前 20 s内 PCl5(g)的平均反应速率为
(2)373K时该反应的平衡常数的值为
(3)若在此平衡体系中再加入 1mol的 PCl5,与原平衡比较,新平衡时 PCl5的转化率 (填“增大”或“减小”,下同)。PCl5的平衡浓度 。
(4)将原平衡升温至 473K,重新达平衡时(其他条件不变),PCl3的平衡浓度为 PCl5的3倍,该反应的正反应为(填“放热反应”或 “吸热反应”) ,为增大平衡体系中 Cl2的物质的量,下列措施正确的是(其它条件相同)
a.升高温度 b.扩大容器的体积
c.加入合适的催化剂 d.再充入 PCl3
查看答案和解析>>
科目: 来源: 题型:
某溶液里加入过量氨水或过量NaOH溶液均有沉淀产生,若加入铁粉或铜粉溶液质量都增加,则溶液中可能含有下列离子的 ( )
A、Al3+ B、Fe2+ C、Fe3+ D、Mg2+
查看答案和解析>>
科目: 来源: 题型:
下表中,甲、乙、丙、丁、戊分别代表一种物质,相邻的物质间在一定条件下能发生反应,不相邻物质间不能发生反应的一组是 ( )
| 选项 | 甲 | 乙 | 丙 | 丁 | 戊 |
| A | SiO2 | CaCO3 | 稀HNO3 | Ag | CuSO4溶液 |
| B | O2 | Fe | 稀H2SO4 | NaOH溶液 | CO2 |
| C | Cl2 | H2S | 稀HNO3 | Al(OH)3 | NaOH溶液 |
| D | CO2 | Mg | 稀HCl | CaO | Na2CO3溶液 |
查看答案和解析>>
科目: 来源: 题型:
有8 g Na2O2、Na2O、Na2CO3、NaOH的混合物与200 g质量分数为3.65%的盐酸恰好反应,蒸干溶液,最终得固体质量为
A.8 g B.15.5 g C.11.7 g D.无法计算
查看答案和解析>>
科目: 来源: 题型:
用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出反应的离子方程式。
(1)FeSO4(CuSO4):
所需试剂(填化学式) ,所涉及的离子方程式: 。
(2)O2(CO2):
所需试剂(填化学式) ,所涉及的离子方程式: 。
查看答案和解析>>
科目: 来源: 题型:
(1)用标准NaOH溶液滴定未知浓度的盐酸,用酚酞作指示剂,下列操作中会导致实验结果偏低的是 。
①碱式滴定管用蒸馏水洗净后没有用标准液润洗
②用酸式滴定管加待测液时,刚用蒸馏水洗净后的滴定管未用待测液润洗
③锥形瓶用蒸馏水洗净后没有用待测液润洗
④滴定前滴定管尖端有气泡,滴定后气泡消失
⑤终点读数时俯视,其他读数方法正确
(2)有一学生在实验室测某溶液的pH。实验时他先用蒸馏水湿润pH试纸,然后用洁净的玻璃棒蘸取试样进行检测。
①该学生的操作 (填“正确”或“不正确”),如不正确,请分析是否一定有误差并说明理由(若正确则此问不用作答)
。
②若按此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 ,原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com