
科目: 来源: 题型:
下列说法中正确的是:
A.氧化剂本身发生氧化反应 B.氧化还原反应一定有氧元素参加
C.氧化剂在反应中得电子,还原剂失去电子 D.氧化反应一定先于还原反应发生
查看答案和解析>>
科目: 来源: 题型:
下列关于镁和钠的比较,结论正确的是
A.铝镁合金的硬度较大,钠钾合金的硬度较小
B.因为钠的金属性比镁要强,所以钠的熔点比镁要高
C.镁能置换硫酸铜中的铜,钠也能置换硫酸铜中的铜
D.在空气中都能被点燃,生成的产物都是氧化物
查看答案和解析>>
科目: 来源: 题型:
在某无色强碱性溶液中,下列各组离子能大量共存的是 高考
A.Na+、K+、AlO2-、Cl- B.Cu2+、Na+、NO3-、SO42-
C.Na+、K+、Cl-、HCO3- D.Ba2+、Na+、NO3-、SO42-
查看答案和解析>>
科目: 来源: 题型:
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
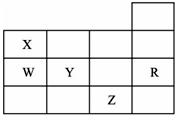
A. 常压下五种元素的单质中Z单质的沸点最高
B. Y、Z的阴离子电子层结构都与R原子的相同
C. W的氢化物的沸点比X的氢化物的沸点高
D. Y元素的非金属性比W元素的非金属性强
查看答案和解析>>
科目: 来源: 题型:
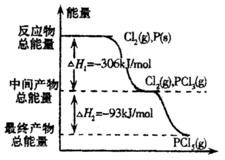
如图是红磷P(s)和Cl2(g)发生反应生成![]() 和
和![]() 的反应过程和能量关系图。其中
的反应过程和能量关系图。其中![]() 分解成
分解成![]() 和
和![]() 的反应是一个可逆反应,温度t℃时,在密闭容器中加入0.6
的反应是一个可逆反应,温度t℃时,在密闭容器中加入0.6![]() ,达平衡时
,达平衡时![]() 还剩0.45mol,其分解率为
还剩0.45mol,其分解率为![]() ,则下列推断不正确的是
,则下列推断不正确的是
A. ![]() 等于25%
等于25%
B.若升高温度,平衡时![]() 的分解率大于
的分解率大于![]()
C.若超始时加入![]() 和0.
和0.![]() ,以相同条件进行反应,则平衡时
,以相同条件进行反应,则平衡时![]() 转化率为3
转化率为3![]()
D. ![]() 分解的热化学方程式为
分解的热化学方程式为![]()
查看答案和解析>>
科目: 来源: 题型:
常温下,在27.5g水中溶解12.5g CuSO4·5H2O,恰好达到饱和,该溶液密度为1.21g /cm3,求:
① 该溶液中阴阳离子的总物质的量
② 该溶液中CuSO4的物质的量浓度
③ 取出20.0 ml该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是多少毫升?
查看答案和解析>>
科目: 来源: 题型:
(1)在25℃条件下将pH=11的氨水稀释100倍后溶液的pH为(填序号)__ __。
A.9 B.13 C.11~13之间 D.9~11之间
(2)25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号)__ ___。
A.氨水与氯化铵发生化学反应; B.氯化铵溶液水解显酸性,增加了c(H+);
C.氯化铵溶于水,电离出大量铵离子,抑制了氨水的电离,使c(OH―)减小;
(3)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),
①__ _、_ __和_ __三种粒子的物质的量之和等于0.1mol。
②_ __和_ __两种粒子的物质的量之和比OH―多0.05mol。
查看答案和解析>>
科目: 来源: 题型:
某课外活动小组为探究CO2与过量的NaOH溶液确实发生了化学反应,甲、乙、丙三位同学设计了下列三种实验装置,请回答下列问题:

(1)甲装置中CO2与过量的NaOH反应的离子方程式 。
(2)丙装置实验现象是 ,解释产生该实验现象的原因
。
(3)甲、乙、丙同学设计的三个方案中,有一个方案在实际操作中安全性存在问题,该方案是 (填甲、乙或丙),原因是
。
(4)请设计一个实验检验生成的产物Na2CO3中的阴离子。(简述操作步骤、所用试剂、实验现象和结论。)
(5)实验室中若需用44.8 L(标准状态)CO2 ,现用含CaCO3 90%石灰石与足量的盐酸反应,至少需要这种石灰石 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com