
科目: 来源: 题型:
根据元素周期表及周期律的知识回答下列问题:
(1)与钠同周期且单质熔点最高的元素位于周期表的第_________周期第_________族。
(2)金属钠在一定条件下可与氢气反应生成氢化钠(2Na+H22NaH)。生成物氢化钠的电子式为________,含有的化学键为_____键(填“离子”、“共价”或“金属”)。
(3)元素周期表中元素的性质存在递变规律,下列比较正确的是??????________。
a.离子半径:Na+>Mg2+>S2->Cl-
b.酸性:H4SiO4>H3PO4>H2SO4>HClO4
c.氢化物稳定性:PH3<H2S<HCl
d. 还原性:PH3>H2S>HCl>HF
(4)第三周期元素的气态原子失去最外层一个电子所需能量(设为E)如下图所示:

① 同周期内,随着原子序数的增大,E值变化的总趋势是__________________。
② 根据上图提供的信息,试推断E氟_______E氧(填“>”“<”或“=”)。
查看答案和解析>>
科目: 来源: 题型:
被誉为“光纤之父”的华人科学家高锟荣获2009年诺贝尔化学奖。下列叙述错误的是( )
A.SiO2是生产光导纤维的主要原料
B.SiO2与CO2(干冰)的晶体结构不同
C.干冰和SiO2固体熔化时破坏的作用力是相同的
D.二氧化硅晶体中不存在SiO2分子,因为它含有类似金刚石的空间网状结构
查看答案和解析>>
科目: 来源: 题型:
已知热化学方程式:SO2(g)+1/2O2 (g)![]() SO3(g) △H=-98.32kJ??mol—1,
SO3(g) △H=-98.32kJ??mol—1,
在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
A.196.64kJ B.98.32kJ C.<196.64kJ D.>196.64kJ
查看答案和解析>>
科目: 来源: 题型:
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图,下列表述中正确的是 ( )
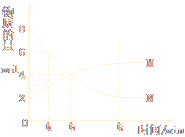
A.反应的化学方程式为:2M![]() N B.t2时,正逆反应速率相等,达到平衡
N B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率 D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目: 来源: 题型:
 下表为元素周期表的一部分。请回答下列问题:
下表为元素周期表的一部分。请回答下列问题:
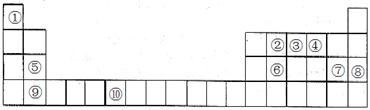
(1)上述元素中,属于s区的是________________________(填元素符号)。
(2)写出元素⑩的基态原子的电子排布式___________________________。
(3)元素第一电离能为⑤________________________⑨(填“大于”或“小于”)。
(4)元素③气态氢化物的中心原子有________________________对弧对电子,其VSEPR模型为________________________;中心原子的杂化类型为_______________;该分子为_________________分子(填“极性”或“非极性”)。向AgNO3溶液中逐滴加入其水溶液,可观察到的现象为_____________ ___________。
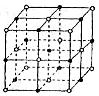
(5)元素⑦的钠盐晶胞结构如上图所示,每个Na+周围与之距离最近的Na+的个数为________________________。若设该晶胞的棱长为a cm,阿伏加德罗常数的值为NA,则该钠盐的密度为________________________(写出计算式)。
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A. HF、HCl、HBr、HI的熔点沸点依次升高。
B. H2O的熔点、沸点大于H2S的是由于H2O分子之间存在氢键。
C. 乙醇分子与水分子之间只存在范德华力。
D. 氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4
查看答案和解析>>
科目: 来源: 题型:
把500 ![]() 有
有![]() 和
和![]() 的混合溶液分成5等份,取一份加入含
的混合溶液分成5等份,取一份加入含![]()
![]() 硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含
硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含![]()
![]() 硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为
硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为
A.![]() B.
B.![]()
C.![]() D.
D.![]()
查看答案和解析>>
科目: 来源: 题型:
2010年在上海举办的世博会将主打环保牌,20辆氢燃料电池公交车、300辆氢燃料电池出租车将投入运行,它们以氢气为能源,实现了真正的零污染。氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是
A.正极反应式为:O2+2H2O+4e-=4OH-
B.工作一段时间后,电解液中KOH的物质的量浓度不变
C.该燃料电池的总反应方程式为:2H2+O2=2H2O
D.用该电池电解CuCl2溶液,产生2.24LCl2(标准状况)时,有0.2mol电子转移
查看答案和解析>>
科目: 来源: 题型:
下列有关实验操作的叙述正确的是( )
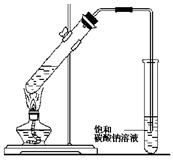
A.实验室常用上图所示的装置制取少量的乙酸乙酯。
B.用50mL酸式滴定管可准确量取 25.00mLKMnO4 溶液
C.用量筒量取5.00 mL1.00mol·L-1盐酸于50mL 容量瓶
中,加水稀释至刻度,可配制0.100mol·L-1盐酸。
D.用苯萃取溴水中的溴,分液时有机层从分液漏斗
的下端放出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com