
科目: 来源: 题型:
已知25 ℃、101 kPa下,石墨、金刚石燃烧的热化学方程式分别为:
C(石墨)+O2(g)=CO2(g) △H=-393.51 kJ·mol-1
C(金刚石)+O2(g)=CO2(g) △H=-395.41 kJ·mol-1
据此判断,下列说法中正确的是。
A.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低
B.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高
C.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低
D.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高
查看答案和解析>>
科目: 来源: 题型:
某有机物的结构是:关于它的性质的描述正确的是( )
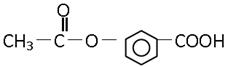
①能发生加成反应; ②能溶解于NaOH溶液中; ③能水解生成两种有机物;
④不能使溴水褪色; ⑤能发生酯化反应; ⑥有酸性
A.①②③ B.②③⑤ C.仅⑥ D.全部正确
查看答案和解析>>
科目: 来源: 题型:
常见镍氢电池的某极是储氢合金LaNi5H6(LaNi5H6中各元素化合价均为零),电池反应通常表示为:LaNi5H6+6NiO(OH) ![]() LaNi5+6Ni(OH)2,下列说法不正确的
LaNi5+6Ni(OH)2,下列说法不正确的
A.放电时储氢合金作正极
B.放电时负极反应:LaNi5H6 + 6OH- - 6e- = LaNi5 + 6H2O
C.充电时阳极周围c(OH-)增大
D.充电时储氢合金作阴极
查看答案和解析>>
科目: 来源: 题型:
可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是
A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O2+2H2O+4e-=4OH-
B.以NaOH溶液为电解液时,负极反应为:Al+3OH--3e=Al(OH)3↓
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
查看答案和解析>>
科目: 来源: 题型:
铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)Fe是人体不可缺少的微量元素,摄入含铁化合物可补充铁。正常人每天应补充14mg左右的铁。其中绝大部分来自于食物。如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天服需用含 mg FeSO4·7H2O的片剂。
(2)某同学为了检验家中的一瓶补铁药(成分为FeSO4)是否变质,查阅了有关资料,得知Fe2+能被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,并结合已学的知识设计了如下实验:将药片除去糖衣研细后,溶解过滤,取滤液分别加入两支试管中,在一支试管中滴入酸性高锰酸钾溶液,在另一支试管中滴入KSCN溶液。该同学观察到的现象是:滴入酸性高锰酸钾溶液后褪色,滴入KSCN溶液后不变红,据此得出的结论是 。
(3)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2![]() 6SO2+Fe3O4,若有3 mol FeS2参加反应,则转移 mol电子。
6SO2+Fe3O4,若有3 mol FeS2参加反应,则转移 mol电子。
(4)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为 ;
(5)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是 。
查看答案和解析>>
科目: 来源: 题型:
如图,将铜片和锌片焊接在一起组成A电极,B为碳棒进行电解实验,电解液中含硝酸银和硝酸铜各0.1 mol。已知电路中通过0.2 mol电子。

(1)请写出A.B两极发生反应的电极反应式A: B:
(2)请分析A.B两极质量变化情况为 A: B:
查看答案和解析>>
科目: 来源: 题型:
某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为45.3g的该结晶水合物,分别制成溶液。向其中一份逐滴加入NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多,一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到2.24L该气体(标准状况),最后白色沉淀逐渐减少并最终消失;另一份逐滴加入Ba(OH)2溶液,开始现象类似,但最终仍有白色沉淀,过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.6 g。
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子和一种阴离子是 。
(2)试通过计算确定该结晶水合物的化学式 。
(3)写出加入过量的Ba(OH)2溶液发生的离子反应方程式: ;
(4)假设过程中向该溶液中加入的Ba(OH)2溶液的物质的量浓度为2.0mol·L-1。则加入 mL Ba(OH)2溶液时,所得沉淀的总物质的量最大。
查看答案和解析>>
科目: 来源: 题型:
![]() 和
和![]() 是氧元素的两种核素,
是氧元素的两种核素,![]() 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是
A.![]() 与
与![]() 互为同分异构体
互为同分异构体
B.![]() 与
与![]() 核外电子排布方式不同
核外电子排布方式不同
C.通过化学变化可以实现![]() 与
与![]() 间的相互转化
间的相互转化
D.标准状况下,1.12L![]() 和1.12L
和1.12L![]() 均含0.1
均含0.1![]() 个氧原子
个氧原子
查看答案和解析>>
科目: 来源: 题型:
下列变化不能说明一定发生了化学变化的是( )
A.变化时有电子的得失或共用电子对的形成 B.变化过程中有化学键的断裂和形成
C.变化时释放出能量
D.变化前后原子的种类和数目不变,分子种类增加
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com