
科目: 来源: 题型:
元素性质呈现周期性变化的根本原因是
A.元素的相对原子质量递增,量变引起质变
B.元素原子的核外电子排布呈周期性变化
C.元素的原子半径呈周期性变化 D.元素的化合价呈周期性变化
查看答案和解析>>
科目: 来源: 题型:
(8分)盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就三大酸与金属反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解,并得到蓝色溶液。该反应的化学方程式为:_________________。
(2)在一定体积的18 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,若被还原的硫酸为0.9mol。则浓硫酸的实际体积_________(填“大于”、“等于”或“小于”)100mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为__________________________________。
(3)根据下图操作及现象推断酸X为______________(填序号)。

浓盐酸 b、浓硫酸 c、浓硝酸
查看答案和解析>>
科目: 来源: 题型:
动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。 |
| ②向新制的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色[来 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| ④将镁条投入稀盐酸中 | D.反应较快,产生无色气体。 |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉锭。 |
查看答案和解析>>
科目: 来源: 题型:
以下关于元素周期表的结构叙述正确的是
A.有七个主族,八个副族
B.有三个长周期(均含18种元素),三个短周期(均含8种元素)
C.零族位于元素周期表的第18列(从左往右)
D.第三主族位于元素周期表的第三列(从左往右)
查看答案和解析>>
科目: 来源: 题型:
物质的量相等的CO和CO2相比较,下列有关叙述中正确的是
①它们所含的分子数目之比为1∶1 ②它们所含的氧原子数目之比为1∶2
③它们所含的原子总数目之比为2∶3 ④它们所含的碳原子数目之比为1∶1
A.①和④ B.②和③ C.④和⑤ D.①②③④
查看答案和解析>>
科目: 来源: 题型:
常温时,下列各组离子在指定溶液中能大量共存的是
A.pH = 1的溶液中:Fe2+、NO3-、SO42-、Na+
B.c(Fe3+) = 0.1 mol/L的溶液中:K+、ClO-、SO42-、SCN-
C.c(H+)/c(OH-) = 1012的溶液中:NH4+、Al3+、NO3-、Cl-
D.由水电离的c(H+) = 1×10-14 mol/L的溶液中:Ca2+、K+、Cl-、HCO3-
查看答案和解析>>
科目: 来源: 题型:
铁与HNO3作用时,还原产物除与HNO3浓度有关外,还与温度有关。已知铁与冷的稀HNO3反应时,主要还原产物为NO气体;与热的稀HN03反应时,主要还原产物为N2O气体;当HNO3更稀时,其重要还原产物是NH4+。现有铁与稀 HNO3的作用,请分析下图,回答有关问题。
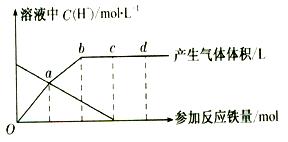
假设曲线的各段内只有一种还原产物,。
(1)0点到a点的还原产物是 。
(2)a点到b点的还原产物是__ __,其原因是 。
(3)试完成b点到c点的反应方程式:
口Fe+口HNO3——口Fe( NO3)3+口[ ]+口H20。
(4)反应过程中,到达 点时,HN03已完全反应。
(5)已知达到d点时反应结束,此时溶液中的主要阳离子是 。
(6)c点和d点参加反应的铁的物质的量之比是 。
查看答案和解析>>
科目: 来源: 题型:
0.2 molX元素的离子被还原成中性原子时,需要得到2.408×1023个电子,0.3gX的单质与足量盐酸反应放出0.015g氢气;X的中子数和质子数相等;Y的原子半径是其所在周期元素中最小的,它的阴离子结构与氩原子结构相同。
(1)计算X的相对原子质量(写出计算过程)
(2)推断X、Y两元素在周期表中的位置。
(3)用化学方程式表示X最高价氧化物对应的水化物与Y单质的反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com