
科目: 来源: 题型:
能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I: CO(g) + 2H2(g) ![]() CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II: CO2(g) + 3H2(g) ![]() CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
① 上述反应符合“原子经济”原则的是 (填“I”或“Ⅱ”)。
② 下表所列数据是反应I在不同温度下的化学平衡常数(K)。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
由表中数据判断ΔH1 0 (填“>”、“=”或“<”)。
③ 某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH = -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH = -566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
请计算1 mol甲醇不完全燃烧生成1 mol一氧化碳和液态水放出的热量为 。
(3)某实验小组依据甲醇燃烧的反应原理,设计如右图所示的电池装置。
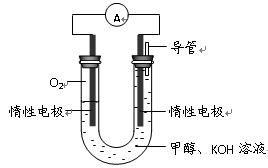
①该电池正极的电极反应为 。
②工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为
。
查看答案和解析>>
科目: 来源: 题型:
已知X、Y、Z、W是短周期元素中的四种非金属元素,它们的原子序数依次增大。X、Y、Z的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍。
(1)Z分子的电子式为: ;Y的单质有多种,其中可以导电的一种是: 。
(2)在一定条件下,由x单质与z单质反应生成1molE放出的热量为46.2kJ,写出该反应的热 化学方程式: ;E在催化剂存在的条件下,可用于还原汽车尾气中的 ,以减少对大气的污染。
(3)仅由X、Z、W三种元素组成的某种盐是一种速效化肥,但长期施用会使土壤酸化,有关的离子方程式为 。
(4)工业上可用E的浓溶液来检验输送氯气的管道是否漏气,若漏气时可观察到大量白烟,同时有单质z生成,写出相应的化学方程式: 。该反应中被氧化的E与参与反应的E的质量之比为 。
查看答案和解析>>
科目: 来源: 题型:
第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图。
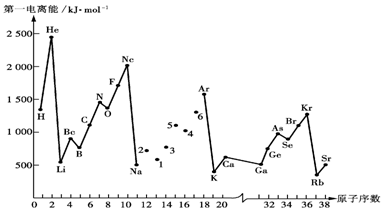
请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,将Na——Ar之间六种元素用短线连接起来,构成完整的图像。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是
。
(3)上图中6号元素在周期表中的位置是 ;其原子M层电子的轨道表示式为 。
(4)上图中4,5,6三种元素的气态氢化物的沸点均比同主族上一周期的元素气态氢化物低很多,原因是: 。
查看答案和解析>>
科目: 来源: 题型:
A是烃的含氧衍生物。为了测定其分子组成,进行如下实验:
①在一定温度和压强下将A气化,其气体的质量是同温、同压下等体积氦气质量的38倍;②称取7.6gA,在11.2L氧气中完全燃烧,其产物只有CO2和水蒸气。将反应后的混合气通过浓硫酸后气体总的物质的量为0.475mol,浓H2SO4质量增加3.6g。再将余下的气体通过盛有足量Na2O2的干燥管后,气体的物质的量减少至0.275mol(气体体积均在标准状况下测定)。
试回答:
(1)A的化学式为_____________。
(2)A物质中只有一条支链,遇FeCl3溶液无显色反应。1molA只能与1molNaOH反应;1molA与足量Na反应生成1molH2。则A的结构简式为__________________。
查看答案和解析>>
科目: 来源: 题型:
新兴的大脑营养学研究发现,大脑的生长发育与不饱和脂肪酸有密切的关系,从深海鱼油中提取的,被称为“脑黄金”的DHA就是一种不饱和程度很高的脂肪酸,它的分子中含6个碳碳双键,化学名称为二十二碳六烯酸,则它的分子组成应为:( )
A.C22H39COOH B.C21H42COOH C.C22H33COOH D.C21H31COOH
查看答案和解析>>
科目: 来源: 题型:
右图为电解饱和食盐水的简易装置,下列有关说法正确的是 ( )
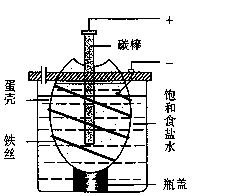 A.电解一段时间后,往蛋壳内溶液中滴加几滴
A.电解一段时间后,往蛋壳内溶液中滴加几滴
酚酞,呈红色
B.蛋壳表面缠绕铁丝发生氧化反应
C.铁丝表而生成的气体能使湿润的淀粉碘化钾
试纸变蓝
D.蛋壳可阻止生成的氯气与氢气、氢氧化钠溶
液接触
查看答案和解析>>
科目: 来源: 题型:
某研究小组为了探究“铁与水蒸气”能否发生反应及反应的产物,进行了系列实验。
(1)用下图所示实验装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”(石棉绒是耐高温材料,不与水反应)。反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当
时(填实验现象),说明“铁与水蒸气”能够进行反应。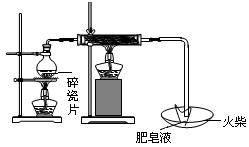
(2)为了研究一定时间内铁粉的转化率,他们设计了如下实验:准确称取一定质量的铁粉进行反应,收集并测量反应后生成的气体体积,计算出铁粉的转化率。
①收集并测量气体体积应选右图中的________装置(填A或B)。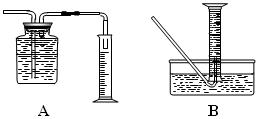
②称取0.24g铁粉与适量石棉绒混合,然后加热至无气体放出。若室温下氢气密度约为0.088g/L,最好选用 规格的量筒(选填字母序号)
A.100mL B.200mL C.500mL D.1000mL
③收集的气体体积为VL,铁粉的转化率为 。
(3)为了证明反应后的固体混合物中含有+3价的Fe,他们计划取出少量混合物于试管中,加入足量的盐酸,溶解、过滤。向滤液中滴加KSCN溶液,观察溶液的颜色。在下表中填写滴加KSCN溶液后可能观察到的现象、结论与解释(可以不填满)。
| 现象 | 结论与解释 | |
| 可能① | ||
| 可能② |
查看答案和解析>>
科目: 来源: 题型:
“神舟七号”宇宙飞船的能量部分来自太阳能电池,另外内部还配有高效的MCFC型燃料电池。该电池可同时供应电和水蒸气,所用燃料为氢气,另一极通入O2和CO2的混合气体,电解质为熔融的碳酸钾。已知该电池的总反应为2H2+O2=2H2O,则下列推断中,正确的是
A.电池工作时,CO32—向正极移动
B.电池放电时,负极反应为H2+CO32—-2e—=CO2↑+H2O
C.正极的电极反应为: O2+2H2O+4e— =4OH—
D.通氧气的电极发生氧化反应
查看答案和解析>>
科目: 来源: 题型:
下列各组离子能在指定溶液中,能大量共存的是( )
①无色溶液中:K+,Cl-,Ca2+,CO32??,SO42??,NO3-
②pH=11的溶液中:CO32-,Na+,AlO2??,NO3??,S2-,SO32-
③水电离的H+浓度c(H+)=10-12mol·L-1的溶液中:Cl-,CO32-,NO3-,NH4+,SO32-
④加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-
⑤使石蕊变红的溶液中:Fe2+,MnO4-,NO3-,Na+,SO42??
⑥中性溶液中:Fe3+,Al3+,NO3-,I??,Cl????????,S2??
A.②④ B.②⑤ C.①③⑥ D.①②④
查看答案和解析>>
科目: 来源: 题型:
短周期元素A、B、C、D、E原子序数依次递增,A原子最外层电子数是次外层电子数的2倍,B的单质为双原子分子,其氢化物能使湿润的石蕊试纸变蓝,C在同周期元素中原子半径最大,D的最外层电子数等于电子层数,E的最高正价是+7价。
(1)写出E元素在周期表中的位置
(2)写出A元素气态氢化物的结构式
(3)B的氢化物和E的氢化物反应所得生成物的电子式为 。
(4)D单质和C的最高价氧化物对应的水化物的溶液反应的离子方程式为
(5)A单质与B的最高价氧化物对应的水化物的浓溶液反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com