
科目: 来源: 题型:
自洁面料就是在普通的面料纤维中加入一层薄薄的纳米二氧化钛。含有Fe2O3的钛铁矿(主要成分为FeTiO3)制取纳米级TiO2的流程如下:
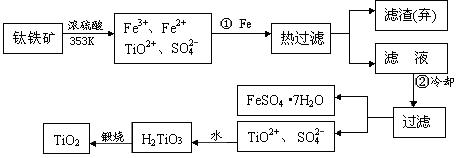
(1)Ti的原子序数为22,Ti位于元素周期表中的第________周期,第______族。
(2)步骤①加铁的目的是_________________;步骤②冷却的目的是_______________。
(3)上述制备二氧化钛的过程中,可以利用的副产物是______________;考虑成本和废物综合利用因素,废液中应加入___________________处理。
(4)由金红石制备单质钛,涉及到的步骤为:
TiO2![]() TiCl4
TiCl4![]() Ti
Ti
已知:①C(s)+O2(g)==CO2(g) △H= -393.5kJ·mol-1
②2CO(g)+O2(g)==2CO2(g) △H= -5665kJ·mol-1
③TiO2(s)+2Cl2(g)==TiCl4(s)+O2(g) △H= +41kJ·mol-1
则TiO2(s)+ 2Cl2(g)+C(s)==TiCl4(s)+2CO(g)的△H=____________。
反应TiCl4+2Mg == 2MgCl2+Ti 在氩气氛中进行的理由是________________________。
查看答案和解析>>
科目: 来源: 题型:
据报道,最近摩托罗拉公司研发出一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:![]() ,则下列说法错误的是( )
,则下列说法错误的是( )
A.放电时![]() 参与反应的电极为正极
参与反应的电极为正极
B.充电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应为:![]()
D.充电时每生成1 mol![]() 转移6 mol电子
转移6 mol电子
查看答案和解析>>
科目: 来源: 题型:
如图表示某因态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4︰5,化合物D是重要的工业原料。
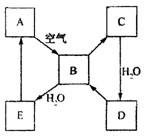
(1)写出A在加热条件下与![]() 反应的化学方程式
反应的化学方程式
________________________________。
(2)写出E与A的氢化物反应生成A的化学方程式
_______________________________________________________________。
(3)写出一个由D生成B的化学方程式
_______________________________________________________________。
(4)将![]() 的E溶液与
的E溶液与![]() 的
的![]() 溶液混合。
溶液混合。
①写出反应的离子方程式_______________________________________________。
②反应后溶液的pH ___ 7(填“大于”、“小于”或“等于”),理由是_______________。
③加热反应后的溶液,其pH___(填“增大”、“不变”或“减小”),理由是_________。
查看答案和解析>>
科目: 来源: 题型:
![]() 表示阿伏加德罗常数,下列有关叙述正确的是
表示阿伏加德罗常数,下列有关叙述正确的是
A.2.0 g![]() 中所含中子数为
中所含中子数为![]()
B.1 L![]() 溶液中
溶液中![]() 的数目为
的数目为![]()
C.标准状况下,1 L辛烷完全燃烧后,所生成气态产物的分子数为![]()
D.含1 mol碳原子的金刚石中,C—C共价键数为![]()
查看答案和解析>>
科目: 来源: 题型:
设NA代表阿伏加德罗常数,下列说法正确的是
A.标准状况下,22.4 LNO和11.2LO2混合后气体的分子总数为1.5 NA
B.200mLlmol·L-1H2SO4溶液含阴、阳离子总数一定为0.6NA。
C.124g白磷分子中含P一P键数目4NA
D.等质量的Mg、Al与足量盐酸反应时产生气体的分子数之比为3︰4
查看答案和解析>>
科目: 来源: 题型:
(14 分)为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
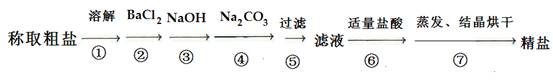
(1)判断BaCl2 已过量的方法是____________________________
(2)第④步中,相关的离子方程式是____________________________
(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是______________
(4)为检验精盐纯度,需配制150mL0.2mol·L-1NaCl(精盐)溶液,如图是该同学 转移溶液的示意图,图中的错误是________________________________。
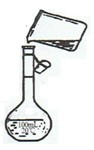
查看答案和解析>>
科目: 来源: 题型:
一切植物中均含有天然有机高分子化合物A,它是构成植物细胞壁的基础物质,不溶于水,也不溶于一般有机溶剂.能发生如下变化(A~F均分别代表一种物质,框图中的部分产物已略去,如:B生成C的同时还有CO2生成.)

(1)由A生成B化学方程式为 .
(2)B、D均含有的官能团是 ,设计实验,用弱氧化剂检验(1)所得到的溶液中
的B分子结构中存在该官能团(要求:所需仪器和药品可以任选,如需采用实验室不
能长期保存的试剂请写出它的制备过程;以下步骤可以不填满.)
①
②
③
④
(3)从A到F发生的反应类型有 .
A.氧化 B.酯化 C.消去 D.水解
(4)写出C到D所发生的化学反应的化学方程式 .
(5)F有多种同分异构体,请写出与它有相同官能团的所有同分异构体
.
查看答案和解析>>
科目: 来源: 题型:
将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是
A.镁比铝活泼,镁失去电子被氧化成Mg2+
B.铝是电池负极,开始工作时溶液中会立即有白色沉淀生成
C.该装置开始工作时,铝片表面的氧化膜可不必处理
D.装置的内外电路中,均是电子的定向移动形成电流
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com