
科目: 来源: 题型:
设NA表示阿伏加德罗常数,下列说法不正确的是
A.16g氧气中所含的氧原子数为NA B.18g水所含电子数为8NA
C.NA个氧气分子和NA个氢气分子的质量比为16∶1
D.常温常压下,11.2LCl2含有的分子数为0.5NA
查看答案和解析>>
科目: 来源: 题型:
我们曾做过a、木炭 b、硫磺 c、红磷 d、铝箔 e、铁丝 在氧气中燃烧的实验。其中产生浓厚的白烟的是 (填序号,下同);发出白光,并且生成能使澄清石灰水变浑浊的是 ;生成物是有刺激性气味的气体的是 ;剧烈燃烧。燃烧生成黑色固体的是 ;燃烧时,必须在集气瓶底装少量水或铺一层细沙的目的是
查看答案和解析>>
科目: 来源: 题型:
(共10分)A、B、C、D、E、F、G是中学里常遇到的一些物质,它们之间有如下转化关系,有些必要的信息已在框图中注明:
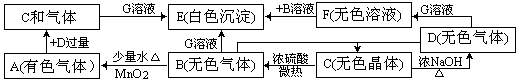
回答下列问题:
(1)D的空间构型为 ,C的电子式为 ,F溶液名称是 ,
(2)在实验室中制取气体A的离子方程式是 .
(3)写出A+D→C的化学方程式 ,
氧化剂与还原剂物质的量之比为 ,
(4)写出:F+B(过量)→E的离子方程式 ,
查看答案和解析>>
科目: 来源: 题型:
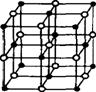 晶体具有规则的几何外形,晶体中最基本的重复单位称晶胞。氯化钠晶体结构如图所示,已知NixO晶体晶胞结构为氯化钠型,由于晶体缺陷,x值小于1,测知NixO晶体的密度为7.4g/cm3,晶胞边长为4.0×10-10m(NA用6.0x1023计算)。试回答(要求计算过程):
晶体具有规则的几何外形,晶体中最基本的重复单位称晶胞。氯化钠晶体结构如图所示,已知NixO晶体晶胞结构为氯化钠型,由于晶体缺陷,x值小于1,测知NixO晶体的密度为7.4g/cm3,晶胞边长为4.0×10-10m(NA用6.0x1023计算)。试回答(要求计算过程):
(1)NixO晶体中的x值_________(精确到0.01)。
(2)晶体中的Ni分别为Ni2+、Ni3+,此晶体化学式____________(用含Ni2+、Ni3+表示)。
查看答案和解析>>
科目: 来源: 题型:
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是 ( )
A.原子半径 A>B>D>C B.原子序数 b> a >d>c
C.离子半径 C>D>B>A D.单质的还原性 A>B>D>C
查看答案和解析>>
科目: 来源: 题型:
(1)由于金属钠很容易与空气中的________、________等物质反应,通常将它保存在__________里。将一小块钠用小刀切开,可以看到表面光亮,但很快变暗,该反应的化学方程式为 ,将一小块钠投入水中,发生反应的化学方程式为 ______________________,在反应后的溶液中加入CuSO4溶液,反应的现象是________________________,
反应的方程式为 ___________________________。
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为:
。
漂白粉的有效成分是(填化学式) 。
查看答案和解析>>
科目: 来源: 题型:
已知A、B、C、D分别是AlCl3、BaCl2、FeSO4、NaOH四种化合物中的一种,它们的水溶液之间的一些反应现象如下: (本题共14分)
① A + B→白色沉淀,加入稀硝酸,沉淀不溶解
② B + D→白色沉淀,在空气中放置,沉淀由白色转化为红褐色
③ C + D→白色沉淀,继续加入D溶液,白色沉淀逐渐消失
⑴试推断A是 B是 C是 D是 。
⑵写出下列反应的离子方程式
A溶液 + B溶液→白色沉淀 ,
C溶液与D溶液反应后生成的白色沉淀溶解于D溶液中
。
查看答案和解析>>
科目: 来源: 题型:
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 。在X极附近观察到的实验现象是 。
②Y电极上的电极反应式为 。检验该电极反应产物的方法是 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应式为 。
②Y电极的材料是 ,电极反应式为 。
(说明:杂质发生的电极反应不必写出)
(3)若要在铁制品表面镀上一层银,则可选用 溶液为电解液,
①X电极的材料是 ,电极反应式为 。
②Y电极的材料是 ,电极反应式为 。
查看答案和解析>>
科目: 来源: 题型:
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫、铁的化合物。
(1)黄铜矿的组成元素中,属于副族元素的是__________(填写名称,下同);属于主族元素的是_____,它位于周期表的位置是__________,它的原子半径________Cl的原子半径(填“>”、“<”或“=”,下同),它的气态氢化物的稳定性____HCl。
(2)冶炼铜的反应为8CuFeS2+21O2![]() 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号),氧化产物是___________(填化学式)。
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:S2O82-+2I-=2SO42-+I2,通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应的催化过程:① (请配平),②S2O82-+2Fe2+=2SO42-+2Fe3+。
查看答案和解析>>
科目: 来源: 题型:
有一混合溶液,其中只含有Fe2+、Cl-、Br-、I-(忽略水的电离),其中Cl-、Br-、I-的个数比为2∶3∶4,向该溶液中通入氯气,使溶液中Cl- 和Br-的个数比为3∶1,则通入氯气的物质的量与溶液中剩余的Fe2+的物质的量之比为( )(还原性I->Fe2+>Br->Cl-)
A.7∶1 B. 7∶3 C. 7∶2 D.7∶4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com