
科目: 来源: 题型:
抗氧剂亚硫酸钠可利用硫酸工业的炉气和尾气与纯碱反应来制取,生产流程如下图:
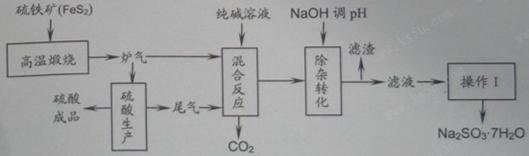
已知:①炉气、尾气中含有SO2;②混合反应中还溶解有少量Fe2O3、MgO等矿尘。
(1)煅烧1molFeS2放出热量为853kJ,则FeS2燃烧的热化学方程式为_____________。
(2)“混合反应”中纯碱(Na2CO3)参与反应的化学方程式为_____________(任写一个)。
(3)用NaOH“除杂”时,主要的离子方程式为_____________(任写一个)。
(4)通过“操作Ⅰ”可以得到亚硫酸钠晶体,写出主要操作步骤的名称:__________。
(3)硫酸生产中炉气转化反应为:2SO2(g)+ O2(g)![]() 2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是________
2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是________
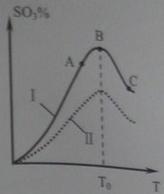
A.该反应的正反应为放热反应
B.曲线Ⅰ上A、C两点反应速率的关系是:![]()
C.反应达到B点时,![]()
D.已知V2O5的催化效果比Fe2O3好,若Ⅰ表示用V2O5催化剂的曲线,则Ⅱ是Fe2O3作催化剂的曲线
查看答案和解析>>
科目: 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.1 L 0.1 mol·L-1 NH4Cl溶液中,NH4+的数目为0.1NA
B.标准状况下,11.2 L的Cl2溶于水,转移的电子总数为0.5NA
C.14 g乙烯、丙烯的混合气体,含有C一H键数为2NA
D.标准状况下,2.24 LCH2Cl2中含有C1原子数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
取两份铝片,第一份与足量盐酸反应,第二份与足量烧碱溶液反应,同温同压下放出相同体积的气体,则两份铝片的质量之比为
A.1:1 B.2:3 C.3:2 D.1:6
查看答案和解析>>
科目: 来源: 题型:
下列各组物质的稀溶液相互反应,把前者逐滴滴入后者与把后者逐滴滴入前者,所产生的现象相同的是
A.AlCl3 和NaOH B.Na2CO3和HCl C.NaAlO2和HCl D.NaCl和AgNO3
查看答案和解析>>
科目: 来源: 题型:
已知某温度下AgCl(s)的溶度积常数Ksp=1×10-10。在该温度下,向50 mL 0.018 mol/L的AgNO3溶液中加入50 mL 0.02 mol/L的盐酸,生成沉淀(混合后溶液的体积变化忽略不计)。下列说法正确的是
A.沉淀生成后,溶液中NO3-的浓度1.8×10-2 mol/L
B.沉淀生成后,溶液的pH为2
C.沉淀生成后,溶液中Ag+的浓度1×10-5 mol/L
D. AgCl的溶解性为难溶,则该物质不溶于水
查看答案和解析>>
科目: 来源: 题型:
用下图装置可以进行测定SO2转化成SO3的转化率的实验。已知SO3的熔点是16.8℃,沸点是44.8℃。已知发生装置中所涉及反应的化学方程式为:
Na2SO3(s) + H2SO4(85%)==Na2SO4 + SO2↑+ H2O
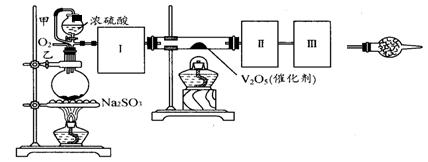
根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~E装置中选择最适合装置并将其序号填入下面的空格中。
Ⅰ、Ⅱ、Ⅲ处连接的装置分别是 、 、 。
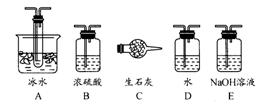
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,首先应采取的操作是 。
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法(可以不填满)。
① 原因 ,验证方法
② 原因 ,验证方法
③ 原因 ,验证方法
(4)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式
(5)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为 %(用含a、b的代数式填写)
查看答案和解析>>
科目: 来源: 题型:
下列各组单质中,前者在一定的条件下能将后者从其化合物中置换出来的是
①Al、Fe ②Cl2、S ③Mg、C ④H2、Cu ⑤C、Si
A. 只有①③ B. 只有②④ C. ①②③④ D. ①②③④⑤
查看答案和解析>>
科目: 来源: 题型:
将SO2通入由CuSO4和NaCl混合的浓溶液中,溶液颜色变浅,析出白色沉淀,取该沉淀进行元素质量分数分析,已知其中含Cl:35.7%,Cu:64.3%,SO2在上述反应中的作用是
A.酸 B.漂白剂 C.还原剂 D.氧化剂
查看答案和解析>>
科目: 来源: 题型:
实验室欲配制100 mL 0.92 mol??L-1的H2SO4溶液(本小题每空2分,共14分)
(1)需要用到的仪器,除了烧杯、空试剂瓶、玻璃棒、量筒、还必须有 ;
(2)若提供的是18.4 mol??L-1的浓H2SO4,求所需量取的浓H2SO4的体积为 mL;
(3)对配制过程中的下列说法,正确的是 。(填序号,多选、少选均不得分)
A.量筒量取浓硫酸后要冲洗并将冲洗液一起倒入小烧杯
B.量好体积的浓硫酸应先倒入小烧杯中然后再加水稀释
C.稀释好的稀硫酸要立即转移入容量瓶
D.若定容后摇匀液面又下降了。则必须再补加水至刻度线。
(4)配制稀硫酸的容量瓶必须洗涤,若用含有蒸馏水的容量瓶未干燥就配制稀硫酸,
则所配稀硫酸浓度将 (偏高、偏低、不变);若用刚配制过NaOH
溶液的容量瓶未洗涤就配制稀硫酸,则所配制的稀硫酸溶液的浓度将
(偏高、偏低、不变);若用刚配制过HCl溶液的容量瓶未洗涤就配制稀硫酸,则
所配制稀硫酸浓度将 (偏高、偏低、不变),
氢离子浓度将 (偏高、偏低、不变)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com