
科目: 来源: 题型:
现有两种不含结晶水的盐,它们在不同温度下的溶解度如下表:
| 20℃ | 50℃ | |
| A的溶解度 | 35.7 g | 46.4 g |
| B的溶解度 | 31.6 g | 108 g |
下列说法中,正确的是
A.可采用重结晶法使A、B混合物分离
B.A的溶解度一定大于B的溶解度
C.20℃时,无法配制30%的A的不饱和溶液
D.将208 g B的饱和溶液降温到20℃,析出76.4 g B
查看答案和解析>>
科目: 来源: 题型:
具有水果香味的中性物质A可以发生下列变化:

(1)推断下述物质的名称
A ___________、B _________。
(2)写出下列变化的化学方程式:
A与NaOH溶液反应 ___________________________________________ ;
D的银镜反应 _________________________________________________ 。
查看答案和解析>>
科目: 来源: 题型:
叠氮酸(HN3)与醋酸酸性相似,下列错误的是
A.HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(N3-)>c(OH-)
B.HN3与NH3作用生成的叠氮酸铵是共价化合物
C.NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3-) >c(OH-)>c(H+)
D.N3-与CO2所含电子数相等
查看答案和解析>>
科目: 来源: 题型:
将 铜和氧化铜的混合物5.8 g加入到过量稀硝酸中,完全反应后产生的气体在标准状况下体积为1.12 L。试计算:
(1)原混合物中CuO的质量分数。
(2)若最初加入的过量稀硝酸浓度为3 mol/L、体积为100 mL,完全反应后溶液的体积仍为100 mL,则该溶液中NO3—的物质的量浓度是多少?
查看答案和解析>>
科目: 来源: 题型:
图表法、图象法是常用的科学研究方法。
I.短周期某主族元素M的电离能情况如图(A)所示。则M元素位于周期表的第 族。
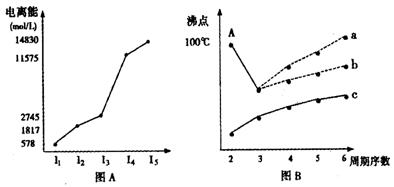
II.图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第 族元素氢化物的沸点的变化规律。不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线——折线a和折线b,你认为正确的是: ,理由是:
。
CH4、NH3、H2O、HF四种氢化物的沸点从高到低的顺序: > > > 。
III.人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属则被科学家预测为是钛(Ti)。钛被誉为“未来世纪的金属”。试回答下列问题:
(1)22Ti元素基态原子的外围电子排布式为 。
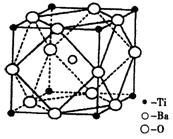
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,介电常数高,是很好的压电材料。偏钛酸钡晶体中晶胞的结构示意图如右图,则它的化学式是 ;每个氧离子周围的钛离子的配位数为 ,每个钡离子周围的氧离子配位数位为 。
查看答案和解析>>
科目: 来源: 题型:
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂;其分子结构如右下图所示。S2Cl2遇水易水解,并产生能使品红褪色的气体。下列说法中错误的是( )

A.S2Cl2固体为分子晶体
B.S2Cl2为含有极性键和非极性键的非极性分子
C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2
D.S2Cl2中硫元素化合价为+1,与H2O反应可能属于氧化还原反应,方程式如下:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com