
科目: 来源: 题型:
某化学兴趣小组参考工业制硝酸的化学原理,在实验室用下列各装置进行组合来制备硝酸并验证硝酸的性质(所给装置必须用到并且只能用一次,各装置中的试剂均足量。已知常温下CaCl2能吸收氨气)。
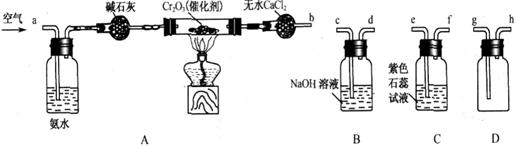
(1)装置的连接顺序为(用a、b、c、d等字母表示):b接( ),( )接( ),( )接( )。
(2)写出氨气催化氧化的化学方程式______________________。
(3)进行实验时,装置A中碱石灰的作用是_____________;D中的现象是_______________。
(4)能证明有硝酸生成的现象是__________________________________________。
(5)实验开始时,下列操作顺序最合理的是______________。
a.先加热A装置中的催化剂.再由导管a通入空气
b.先由导管a通人空气,再加热A装置中的催化剂
c.在由导管a通人空气的同时,加热A装置中的催化剂
查看答案和解析>>
科目: 来源: 题型:
在接触法制硫酸的有关问题中,下列叙述不正确的是
A.燃烧黄铁矿制取SO2的化学方程式是![]()
![]()
![]()
B.含SO2的炉气在进行氧化反应前必须净化,其目的就是为了除尘、以防催化剂中毒
C.用98.3%的浓H2SO4吸收SO3制取发烟硫酸,用稀H2SO4吸收SO3制较浓的H2SO4
D.SO2氧化时必须使用催化剂(例如V2O5等),催化剂的作用是提高SO2的氧化速率,缩短到达平衡所需的时间,但使用催化剂不会提高SO2的转化率
查看答案和解析>>
科目: 来源: 题型:
常温下,在25 mL 0.1 mol·L﹣1 NaOH溶液中逐滴加入a mL 0.2 mol·L﹣1 CH3COOH溶液,有关混合溶液的判断正确的是( )
A.当pH=7时,一定有:c(Na+)=c(CH3COO﹣)=c(OH﹣)=c(H+)
B.当a=25时,一定有:c(CH3COO﹣)+c(CH3COOH)=c(Na+)
C.当c(CH3COO﹣)>c(Na+)时,a一定大于12.5
D.当c(OH﹣)>c(H+)时,a一定小于12.5
查看答案和解析>>
科目: 来源: 题型:
由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是( )
A.②④⑤③① B.③②④①⑤ C.③④②⑤① D.②④③⑤①
查看答案和解析>>
科目: 来源: 题型:
工业上常用废铁屑溶于一定浓度的硫酸溶液制备绿矾( FeSO4·7H2O )。
(1)若用98% 1.84 g/cm3的浓硫酸配制生产用28%的硫酸溶液,则浓硫酸与水的体积比约为1: ▲ 。
(2)为测定某久置于空气的绿矾样品中Fe2+的氧化率,某同学设计如下实验:取一定量的样品溶于足量的稀硫酸中,然后加入5.00 g铁粉充分反应,收集到224 mL(标准状况)气体,剩余固体质量为3.88 g,测得反应后的溶液中Fe2+的物质的量为0.14 mol(不含Fe3+)。则该样品中Fe2+离子的氧化率为 ▲ 。
(3)硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](俗称莫尔盐),较绿矾稳定,在氧化还原滴定分析中常用来配制Fe2+的标准溶液。现取0.4 g Cu2S和CuS的混合物在酸性溶液中用40 mL 0.150 mol/L KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与V mL 0.2 mol/L (NH4)2Fe(SO4)2溶液完全反应。已知:MnO4-+Fe2++H+——Mn2++Fe3++H2O(未配平)
①V的取值范围为 ▲ ;
②若V=35,试计算混合物中CuS的质量分数。
查看答案和解析>>
科目: 来源: 题型:
现有3瓶没有标签的无色溶液,它们分别是NaHCO3、Ba(OH)2、H2SO4
中的各一种,某研究性学习小组探究“不用其它试剂即可鉴别”的方法。将试剂瓶分别编号为①、②、③。
⑴甲同学采用如下实验方案:
分别取样进行分组实验,现象如下表所示:
| ③ | ② | ① | |
| ① | ↑ | ↓ | |
| ② | ↓ | ↓ | |
| ③ | ↓ | ↑ |
根据实验现象得出结论:②试剂为 。
甲同学又做如下两个实验,鉴别①和③

请分析甲同学实验失败的可能原因: 。
⑵乙同学采用如下实验方案:
乙同学采用甲同学同样的实验过程,鉴别出其中的②后,又做如下实验:

请分析乙同学实验失败的可能原因: 。
⑶丙同学采用如下实验方案:
丙同学采用甲同学同样的实验过程,鉴别出其中的②后,又做如下实验:
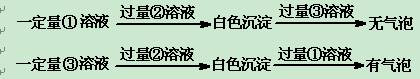
根据实验现象得出结论:①试剂为 ,③试剂为 。
⑷丁同学参与甲、乙、丙三位同学的实验过程,发现当采用分组实验鉴别出②后,无需再进行任何实验操作,立即就可区分出另外两瓶试剂,他的方法是 。
查看答案和解析>>
科目: 来源: 题型:
在下列各组溶液中,离子一定能大量共存的是
A.加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、I-
B.常温下,pH=1的溶液:Fe3+、Na+、NO3-、SO42-
C.滴入酚酞试液显红色的溶液:Mg2+、Al3+、Br-、SO42-
D.含0.1mol/LNH4Al(SO4)2·12H2O的溶液:K+、Ca2+、NO3-、OH-
查看答案和解析>>
科目: 来源: 题型:
某实验小组利用饱和食盐水、导线、直流电源(用“![]() ” 或“
” 或“![]() ”表示)、烧杯、灵
”表示)、烧杯、灵
敏电流计(用“![]() ”表示)和两个电极棒(分别是M、N)进行电化学实验探究。
”表示)和两个电极棒(分别是M、N)进行电化学实验探究。
甲同学安装好仪器,接好直流电源通电几分钟,发现M处溶液逐渐变浅绿色,过一段时间,溶液变得浑浊且逐渐出现红棕色。
乙同学所用的仪器和甲同学的看上去相同,但接好直流电源通电几秒钟,却闻到一股刺鼻的气味,马上停止通电。
丙同学安装好仪器,线路闭合几秒钟后,却没有发现明显现象产生,他又很快接入灵敏电流计,发现电流计的指针发生了偏转。
请根据上述同学的实验现象回答以下问题:
(1)M电极棒材料是(写化学式) ,N电极棒材料是(写化学式) 。
(2)在下列虚框内完成对应三个同学的装置图:
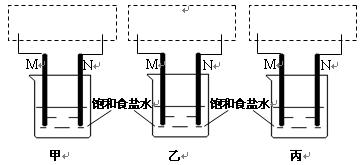
(3)按要求写出三个同学实验过程中涉及的反应方程式:
甲同学N电极方程式
乙同学总反应的离子方程式
丙同学N电极方程式
(4)用化学方程式解释甲同学实验时观察到M处溶液出现浑浊后转为红棕色现象的原因:
。
(5)丙同学为了保护M电极不被腐蚀,他可以将N电极棒更换为(写化学式) 。为验证该防护方法有效,他又做下列对比实验:接通电路2分钟后,分别在M电极区滴入2滴黄色K3[Fe(CN)6]溶液,发现没有更换N电极棒的烧杯中的现象是 。
查看答案和解析>>
科目: 来源: 题型:
如用重结晶法除去某产品中的杂质,为此要选择合适的溶剂,溶剂的下列特点中不可取的是( )
A.杂质在溶剂中的溶解度很大
B.产品在溶剂中的溶解度随温度升高而迅速增大
C.在同一溶剂中,产品比杂质易溶 D.在室温时,产品在溶剂中易溶
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com