
科目: 来源: 题型:
废旧印刷电路板的回收利用可实现资源再生,并减少污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末
(1)废旧印刷电路板中回收的铁是新型电池的使用材料,如制成LiFePO4电池,它可用于电动汽车。电池反应为:FePO4+Li ![]() LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。放电时其正极反应方程式为:
LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。放电时其正极反应方程式为:
(2)用H2O2 和H2SO4 的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H=64.39kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g) △H=-196.46kJ·mol-1
H2(g)+1/2O2(g)=H2O(l) △H=-285.84kJ·mol-1
则在H2SO4 溶液中Cu 与H2O2 反应生成Cu2+和H2O的热化学方程式为: 。
(3)部分金属的回收需要氧化性很强的溶液,如金常用 和 的混合溶液溶解
(4)为了分离金属粉末常用到氰酸(HCN)溶液,HCN是一种有毒且较弱的酸,已知:常温下HCN的电离程度非常小,其Ka=6.2×10-10,0.1mol/L的NaCN的pH=11.1,0.1mol/L的NH4CN的pH=9.2, 则浓度都是0.1mol/L的NaCN和NH4CN溶液中,CN-水解程度大小为:NaCN NH4CN(填:> = < ),理由是:
查看答案和解析>>
科目: 来源: 题型:
在容积为2L的密闭容器中,进行反应:A(g)+2B(g)![]() C(g)+D(g)
C(g)+D(g)
在不同温度下,D的物质的量n(D)和时间t的关系如图所示。试回答下列问题:

(1)800℃时,0—5min内,以B的浓度变化
表示的平均反应速率为 。
(2)能判断该反应达到化学平衡状态的依据
是 。
a.容器中压强不变
b.混合气体中c(A)不变
c.2v正(B)=v逆(D)
d.A、B、C、D四者共存
(3)该反应的正反应为 反应(填吸热或放热);判断的理由是 。
(4)若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K(要求有计算过程)。
查看答案和解析>>
科目: 来源: 题型:
如图所示,向A中充入1 mol X和1 mol Y,向B中充入2 mol X和2 mol Y,起始VA=VB=a L,在相同温度和有催化剂的条件下,两容器内各自发生下列反应:X(g)+Y(g)![]() 2Z(g)+W(g);△H>0,达到平衡时,VA=1.2a L。则下列说法不正确的是
2Z(g)+W(g);△H>0,达到平衡时,VA=1.2a L。则下列说法不正确的是
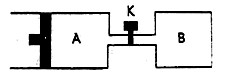
A.反应开始时,B容器中化学反应速率快
B.平衡时,A容器中X的转化率为40%,且比B容器内X的转化率大
C.打开K一段时间再次达到平衡时,A的体积为1.6aL(连通管内体积不计)
D.打开K再次达到平衡后,升高温度,A容器体积会增大
查看答案和解析>>
科目: 来源: 题型:
有A、B、C、D四种化合物,分别由K+、Ba2+、SO![]() 、CO
、CO![]() 、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。请回答:
、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。请回答:
(1)写出化学式:A ; C ;D ;
(2)写出下列反应的离子方程式。
B与盐酸反应 _______________________
E与过量的澄清石灰水反应 ___________________________
查看答案和解析>>
科目: 来源: 题型:
硒(Se)是人体必需的微量元素,它的一种同位素是![]() Se。下列有关该同位素的说法正确的是
Se。下列有关该同位素的说法正确的是
A.质子数为80 B.电子数为114
C.中子数为46 D.质量数为34
查看答案和解析>>
科目: 来源: 题型:
(本题共12分)
以海水中常见物质A为原料可以发展很多种工业,下图中包含了中学课本中介绍的几种基本工业生产,请根据物质之间的转化关系回答下列问题:

(1)C和D、C和G反应都可以制取消毒剂。C和G反应制取的消毒剂中有效成分的化学式为 ;
(2)写出电解A溶液的化学方程式为 ;
(3)若使工业合成J反应的平衡向生成J的方向移动,可采取的措施有 (填字母代号);
A.升高温度 B.增大压强 C.使用催化剂 D.液化分离
(4)将F和J通入A的饱合溶液中的顺序为 。
A.先通入F后通入J B.先通入J后通入F
C.同时通入 D.没有先后顺序要求
(5)图中所示工业制法获得的纯碱中常含有NaCl杂质,用下述方法可以测定样品中
NaCl的质量分数。
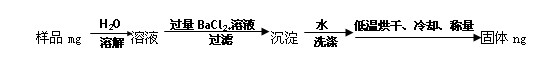 ①检验沉淀是否洗涤干净的所用到的试剂是: ,
①检验沉淀是否洗涤干净的所用到的试剂是: ,
②样品中NaCl的质量分数的数学表达式为: 。
查看答案和解析>>
科目: 来源: 题型:
化学与工农业生产和人类生活密切相关。下列说法中,不正确的是( ) w.w.w.k.s.5.u.c.o.m
A.油脂在碱性条件下水解可制得肥皂
B.海轮外壳上镶入锌块,可减缓船体的腐蚀
C.人体中缺碘元素会得贫血病
D.研制推广甲醇燃料汽车,有利于“减排目标”的实现
查看答案和解析>>
科目: 来源: 题型:
5.25℃时,水的电离可达到平衡:H2O=H++OH-;△H>0,下列叙述正确的是( )
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,Kw增大,pH不变
查看答案和解析>>
科目: 来源: 题型:
为了研究铜与硝酸的反应,化学兴趣小组设计了如下实验装置,其中a、b、c是活塞。
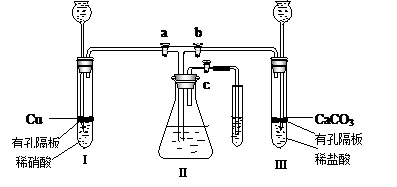 (1)装药品前,按图装置连接后,如何检验气密性?
(1)装药品前,按图装置连接后,如何检验气密性?
(2)按
图装药品后,如果开启 a 和 c ,关闭b ,则Ⅱ中的现象是
;若要使Ⅱ里的气体始终保持无色,应该怎样操作?
写出Ⅰ及Ⅱ中发生的反应的离子方程式:
(3)如果将Ⅰ管中的稀硝酸换成浓硝酸,开启 a 和 c ,关闭 b ,过一会观察,可以看到Ⅱ里没入水中的导管有气泡冒出,导管内气体呈红棕色,液面上方气体为无色,试用文字及方程式解释这一现象 。
(4)在实验(2)中,如果装置Ⅰ、Ⅱ里液面上空间的总体积为Vml,空气中氧气的体积分数为 21%,实验在标准状况下进行,全部氧气通过反应转化为硝酸;实验开始时加入的铜为mg,实验完毕后剩余铜ng,Ⅱ中所得溶液的体积也为Vml(不考虑装置外空气的可能进入)。则Ⅱ中所得溶液的物质的量浓度是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com